
谁在帮助肿瘤"策反"免疫系统?
近年来,免疫治疗成为抗癌领域最受关注的突破之一,但一个现实问题始终困扰医生和患者--为什么同样的免疫治疗,有的人效果显著,有的人却几乎无效?答案很可能藏在肿瘤内部一个"看不见的生态系统"里--肿瘤免疫微环境(tumor immune microenvironment,TIME)。越来越多研究表明,这个微环境的真正"幕后操盘手"其实是肿瘤细胞内部的基因改变。
医肿瘤免疫微环境:真正的抗肿瘤战场
很多人以为肿瘤只是异常增殖的一团细胞,其实不然,肿瘤组织更像一个"小社会",里面有免疫细胞、肿瘤相关成纤维细胞、血管内皮细胞以及多种细胞因子和代谢产物等,这些共同构成了TIME,并决定肿瘤的发展方向和治疗反应。
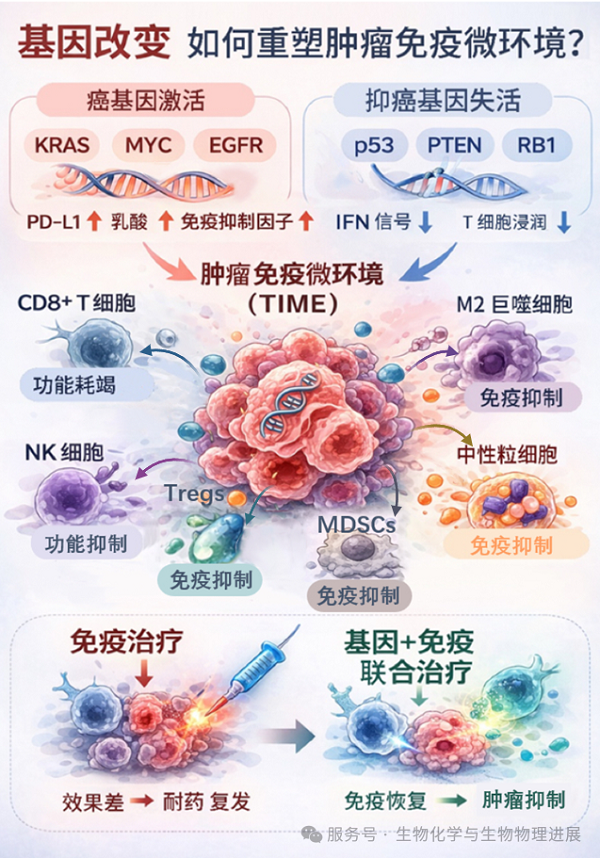
在正常情况下,机体免疫系统能够识别并清除异常细胞,像"警察"一样维持体内秩序。然而,当癌基因异常激活或者抑癌基因功能丧失时,肿瘤细胞不仅获得无限增殖能力,还能通过分泌免疫抑制因子、改变代谢环境和调控免疫检查点分子表达等方式重塑周围微环境,使具有抗肿瘤作用的T细胞、
自然杀伤(NK)细胞等免疫细胞失去杀伤肿瘤细胞的功能,甚至将某些免疫细胞"策反"为促进肿瘤生长的帮手。因此,TIME逐渐从防御屏障转变为肿瘤发展的温床,并成为决定免疫治疗效果的关键因素。
癌基因:把免疫系统变成"帮凶
所谓原癌基因原本是正常存在的"生长调控基因",其一旦发生突变或异常激活就会变成癌基因,推动肿瘤发展[1],常见代表包括KRAS、c-Myc、EGFR 等。
01 癌基因突变:打造免疫"隔离墙"
KRAS突变可以招募髓源性抑制细胞(myeloid-derived suppressor cells,MDSCs)进入肿瘤组织形成免疫抑制屏障[2]。此外,KRAS突变还能够增加乳酸的产生,抑制免疫细胞活性[3],最终导致肿瘤形成一个对免疫系统不友好的"酸性堡垒"。
02 癌基因突变:让肿瘤"隐身"
c-Myc的作用更像"伪装大师",能够降低呈递肿瘤抗原的能力,并上调CD47("别吃我"信号)分子的表达[4],使肿瘤细胞在免疫系统面前几乎"隐形",从而逃逸免疫系统的监视和清除。
03 癌基因突变:全面压制抗肿瘤免疫
EGFR异常可以招募具有促肿瘤作用的M2型巨噬细胞和抑制抗肿瘤免疫应答作用的调节性T细胞(Treg cells),并抑制CD8+T细胞浸润;KRAS、c-Myc与EGFR突变均会上调程序性死亡受体配体1(PD-L1)表达,使T细胞与NK细胞"失去战斗力",相当于给肿瘤打造了一个"免疫防护罩"。
抑癌基因失效:刹车失灵的后果
如果说癌基因是促进肿瘤发生与发展的"油门",那么抑癌基因就是"刹车",一旦失效,后果同样严重,常见抑癌基因包括p53、PTEN、RB1 等。
01 抑癌基因:抗肿瘤免疫的守护者
p53被誉为"基因组守护者",它不仅维持基因组稳定、抑制异常细胞增殖,也参与调控抗肿瘤免疫。当p53功能正常时,可促进免疫系统识别并清除肿瘤细胞,维持免疫微环境的平衡,但当p53突变或失活后,肿瘤会通过招募中性粒细胞和M2型巨噬细胞等促肿瘤免疫细胞[5],减少NK细胞和CD8+ T细胞的浸润等多种方式重塑免疫环境,此外,p53失调还会抑制干扰素(IFN)信号[6],并通过外泌体等方式影响周围基质细胞,进一步推动免疫抑制性肿瘤微环境的形成。
02 抑癌基因:免疫治疗的助力器
抑癌基因在支持抗肿瘤免疫治疗中发挥重要作用。以PTEN为例,当PTEN功能正常时,有助于CD8+ T细胞等免疫细胞进入肿瘤组织,增强免疫治疗效果。相反,当PTEN缺失或功能受损时,肿瘤往往表现为免疫抑制细胞浸润增多,同时PD-L1分子表达升高、血管生成异常等[7],这些改变会削弱免疫系统的攻击能力,并导致免疫治疗的耐药,这也是为什么PTEN状态常被用来预测免疫治疗效果。
从基因入手,打开免疫治疗新思路
随着研究的深入,人们逐渐认识到TIME的异常往往来自于肿瘤细胞内部的基因异常。无论是癌基因异常激活,还是抑癌基因功能丧失,都可能通过多种途径来塑造肿瘤组织免疫抑制性环境,不仅推动肿瘤进展,也直接影响患者对免疫治疗的响应。因此,现代肿瘤治疗理念正在发生重要转变--从单纯激活免疫系统,转向同时纠正肿瘤的基因驱动因素,即从根本上"解除肿瘤对免疫系统的压制"。
基于这一思路,越来越多研究开始探索将靶向异常基因的治疗与免疫疗法联合应用,通过干预关键信号通路重塑TIME、提升免疫治疗的敏感性并克服耐药,这种"基因+免疫"的协同治疗策略,正在成为精准肿瘤治疗的重要方向。
当然,这一领域仍面临挑战。现实中,大多数肿瘤的发生并非由单一基因驱动,而是多种基因异常共同作用的结果,且不同患者之间的TIME差异也十分显著。因此,未来的关键在于精准解析个体基因改变,动态评估TIME状态,制定个体化联合治疗方案。
结 语
癌症,从来不只是细胞增殖失控那么简单,它更像是一场"生态系统重构"。癌基因与抑癌基因就像幕后操控者,通过复杂的信号网络改写免疫系统的行为,帮助肿瘤逃避免疫监视,而理解这些机制,正是走向精准免疫治疗的关键一步。可以预见,随着多组学技术和精准医学的发展,基于肿瘤基因改变的免疫治疗,将为更多患者带来新的希望。(详情请点击阅读原文)
参考文献
[1] Goyns M H, Hancock B W. Importance of oncogene research to the cancer clinician. Clin Oncol (R Coll Radiol), 1991, 3(3): 168-176
[2] Bao Y, Tong C, Xiong X. CXCL3: a key player in tumor microenvironment and inflammatory diseases. Life Sci, 2024, 348: 122691
[3] Chen S, Xu Y, Zhuo W, et al. The emerging role of lactate in tumor microenvironment and its clinical relevance. Cancer Lett, 2024, 590: 216837
[4] Casey S C, Tong L, Li Y, et al. MYC regulates the antitumor immune response through CD47 and PD-L1. Science, 2016, 352(6282): 227-231
[5] Nian Z, Dou Y, Shen Y, et al. Interleukin-34-orchestrated tumor-associated macrophage reprogramming is required for tumor immune escape driven by p53 inactivation. Immunity, 2024, 57(10): 2344-2361.e7
[6] Ho J N H G, Schmidt D, Lowinus T, et al. Targeting MDM2 enhances antileukemia immunity after allogeneic transplantation via MHC-II and TRAIL-R1/2 upregulation. Blood, 2022, 140(10): 1167-1181
[7] Yang S, Pham L K, Liao C P, et al. A novel bone morphogenetic protein signaling in heterotypic cell interactions in prostate cancer. Cancer Res, 2008, 68(1): 198-205
作者简介
金晨晨:山东大学药学院博士生。研究方向为抗肿瘤免疫。
张 建:山东大学药学院教授,博士生导师。研究方向为炎症性疾病与免疫治疗。
(作者:金晨晨、张建)
(本文来源于公众号:生物化学与生物物理进展)
附件下载: