
超声微泡:神经退行性疾病的新希望
随着人口老龄化进程加快,阿尔茨海默病(AD)、帕金森病(PD)和肌萎缩侧索硬化症(ALS,亦称渐冻症)等神经退行性疾病(NDs)的发病人数越来越多,全世界已超过5500万,预计2050年将增至1.5亿,成为影响人民健康的严峻挑战[1]。
大脑的"防盗门":保护还是阻碍?
大脑是人体的"最高司令部",也是脆弱的"易碎品"。为保卫其安全,身体特设了一道精密的防盗门--血脑屏障。这道由毛细血管内皮细胞、基底膜和星形胶质细胞构成的"三重防线"是一道严密的关卡,只允许氧气、二氧化碳和水等小分子自由通过[2]。它保护着中枢神经系统免受病原体和毒素的侵袭,却也让超过98%的小分子药物和几乎100%的大分子药物"吃闭门羹",把绝大多数药物拒之门外[3]。传统的解决方法往往"伤敌一千,自损八百",增加药物透过的同时也可能导致毒素和炎症因子一并涌入,带来更大风险,导致神经退行性疾病的治疗处于"有药难送"的窘境。
超声微泡:一把能打开血脑屏障的神奇钥匙
超声微泡是近年来材料科学与生物工程交叉融合的新兴产物,结合微泡载体和超声波的物理特性,能瞬时可逆打开血脑屏障从而增加药物透过浓度,具有靶向性强、安全性好、非侵入性以及载药性能高等多种优势[4]。在特定频率和强度的超声波作用下,微泡发生振动、膨胀乃至破裂,对周围的血管壁产生微小的机械力,短暂拉开细胞间的紧密连接,从而形成可供药物通过的临时通道[5]。
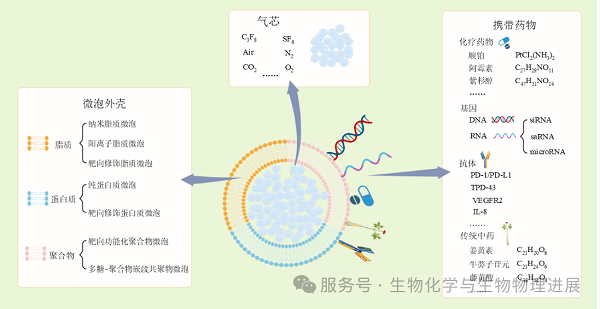
微泡由气体核心及生物相容性外壳两个关键部分组成。气体核心通常填充全氟化碳或六氟化硫,以确保其在血液循环中的稳定性;外壳则由脂质、蛋白质、高分子聚合物等材料构成[6]。得益于这种独特的结构,微泡具有强大的递送潜力,可装载的药物范围广泛,包括传统的化疗药物、中药单体化合物、蛋白质及抗体类药物,以及用于基因治疗的核酸药物[7]。(详情请点击阅读原文)
精准递送:给药物装上"GPS导航"
更巧妙的是,超声微泡不仅能够开启血脑屏障,还能实现"精准送药"。一方面,通过精准调控超声波的聚焦区域,医生可以引导微泡在特定脑区定点释放--例如针对阿尔茨海默病患者的海马区[8],或是帕金森病患者的黑质区域进行靶向给药[9]。另一方面,对微泡进行"功能化升级":在其表面偶联特定的抗体、配体或多肽,使其能够主动识别并结合病灶组织,从而进一步实现细胞乃至分子水平的精准治疗[10]。
智能微泡:未来药物的"变形金刚"
此外,科学家们还赋予微泡更强大的"超能力",他们开发出能够感知内外环境变化并做出响应性反应的智能微泡,例如pH或/和温度响应型微泡可在病灶部位精准释药[11];集成荧光标记的实时可视化微泡,则实现了超声-荧光多模态成像引导下的诊疗一体化[12]。这些创新设计使微泡从单纯的药物载体进化为集靶向识别、智能响应、实时监测与精准治疗于一体的多功能平台,为个性化医疗和精准诊疗开辟了全新的途径。
未来可期:无创精准治疗的新曙光
在不久的将来,随着超声微泡与免疫疗法、干细胞疗法等前沿手段的深度融合,我们或将见证神经退行性疾病病程的逐步延缓甚至逆转。从"有药难送"到智能精准释放,超声微泡技术缩短的不仅是药物与病灶的距离,更是患者与健康生活的距离。
参考文献
1 World Health Organization. Dementia. Geneva: World Health Organization, 2025[2025-03-31]. https://www. who. int/news-room/fact-sheets/detail/dementia
2 Tharakan B. Vascular Hyperpermeability: Methods and Protocols. New York, NY: Springer US, 2024
3 Tashima T, Tournier N. Non-invasive device-mediated drug delivery to the brain across the blood-brain barrier. Pharmaceutics, 2024, 16(3): 361
4 Yang Y, Liu R, Lv H, et al. Targeting tumor stroma via ultrasound-activated nanodroplets: Disrupting exosome-driven microenvironment crosstalk for enhanced antitumor efficacy. J Control Release, 2025, 386: 114113
5 Helfield B, Sirsi S, Kwan J, et al. Cavitation-enhanced drug delivery and immunotherapy. Pharmaceutics, 2023, 15(9): 2207
6 Sharma D, Leong K X, Czarnota G J. Application of ultrasound combined with microbubbles for cancer therapy. Int J Mol Sci, 2022, 23(8): 4393
7 Rastegar G, Salman M M, Sirsi S R. Remote loading: the missing piece for achieving high drug payload and rapid release in polymeric microbubbles. Pharmaceutics, 2023, 15(11): 2550
8 Choi J J, Wang S, Brown T R, et al. Noninvasive and transient blood-brain barrier opening in the hippocampus of Alzheimer's double transgenic mice using focused ultrasound. Ultrason Imaging, 2008, 30(3): 189-200
9 Trinh D, Nash J, Goertz D, et al. Microbubble drug conjugate and focused ultrasound blood brain barrier delivery of AAV-2 SIRT-3. Drug Deliv, 2022, 29(1): 1176-1183
10 Sierra C, Acosta C, Chen C, et al. Lipid microbubbles as a vehicle for targeted drug delivery using focused ultrasound-induced blood-brain barrier opening. J Cereb Blood Flow Metab, 2017, 37(4): 1236-1250
11 Zhao Y, Shi D, Guo L, et al. Ultrasound targeted microbubble destruction-triggered nitric oxide release via nanoscale ultrasound contrast agent for sensitizing chemoimmunotherapy. J Nanobiotechnology, 2023, 21(1): 35
12 Wang J, Wang Y, Jia J, et al. Dual-modality molecular imaging of tumor via quantum dots-liposome-microbubble complexes. Pharmaceutics, 2022, 14(11): 2510
作者简介
郑若泉:三峡大学基础医学院科技创新项目本科生。研究方向:创新药物设计与开发。
李韦民:三峡大学基础医学院临床医学学术型硕士生。研究方向:创新药物设计与开发。
黄益玲:三峡大学基础医学院副教授。研究方向:创新药物设计与开发。
(作者:郑若泉、李韦民、黄益玲)
(本文来源于公众号:生物化学与生物物理进展)
附件下载: