
高璞研究组合作发现2'3'-cGAMP介导的全新膜损伤机制
cGAS-cGAMP-STING通路是动物天然免疫中的经典DNA识别通路,在感染、炎症和肿瘤免疫等过程中发挥重要作用。其中,2'3'-cGAMP作为关键第二信使,负责把上游DNA识别信号传递给下游膜蛋白STING。2'3'-cGAMP备受关注,不仅因为它是动物中首次发现的内源性环二核苷酸,还因为其独特的2'-5'和3'-5'混合磷酸键结构赋予了更强的STING激活能力,并影响了相关激动剂的设计。
2026年4月17日,中国科学院生物物理研究所高璞团队与北京理工大学高昂团队合作,在《Cell》在线发表题为"2'3'-cGAMP-induced membrane shearing promotes broad antiphage immunity"的研究论文。该研究系统解析了2'3'-cGAMP在原核生物中的生成方式、其激活下游跨膜效应蛋白的过程,以及这一信号最终如何导致新型生物膜损伤和细胞死亡。这项工作拓展了我们对天然免疫信号体系演化多样性和膜蛋白破坏生物膜机制的认识。
研究发现,细菌广泛编码的一类CD-NTase在DNA和Mn²⁺存在时会被激活,并特异性合成2'3'-cGAMP。进一步的质谱和核磁共振分析表明,该产物在化学连接方式上与哺乳动物cGAS生成的2'3'-cGAMP一致。这说明,无论是"DNA刺激+Mn??促进"的生成逻辑,还是2'3'-cGAMP本身的特殊结构,都不是动物系统独有,而是在原核生物中同样保守存在,提示这一信号轴具有更古老的演化来源。
在明确上游信号后,研究进一步聚焦一类广泛存在的跨膜效应蛋白-3TM-SAVED。结果显示,这类蛋白在静息状态下以单体存在;在特异性识别2'3'-cGAMP后,会先形成短暂的二聚体中间态,随后进一步组装成高阶纤维。结构与功能分析表明,2'3'-cGAMP在这一过程中并不只是简单的激活配体,而更像连接相邻SAVED结构域的"分子胶水",直接参与并稳定蛋白装配界面,推动蛋白从静息态逐步进入执行激活态。与其他环二核苷酸相比,只有2'3'-cGAMP能够高效触发这一过程,显示出很强的识别特异性。
研究过程中的一个意外且重要的发现,是揭示了一种全新的膜损伤实现模式。不同于传统的打孔、膜溶解或离子通透模式,2'3'-cGAMP诱导形成的高阶纤维会重排自身的跨膜螺旋和两亲性发夹结构,使其以彼此错位的方式共同作用于脂双层,牵引膜沿垂直方向发生上下错位。作者将这种现象概括为"纵向膜剪切"。进一步研究发现,这种剪切并不是单纯的膜形变,而会在扰乱的膜界面形成一串线性排列的小孔。这些小孔足以让水、离子和小分子通过,从而显著提高膜通透性,最终触发细胞死亡并阻断病毒扩增。
综上,这项研究从信号分子、受体机制和效应执行三个层面拓展了我们对天然免疫进化多样性的理解:揭示了2'3'-cGAMP在原核生物中的保守生成机制,阐明了其特异性驱动跨膜效应蛋白变构与高阶装配的过程,并发现了一种此前未被认识的全新膜损伤模式--纵向膜剪切。
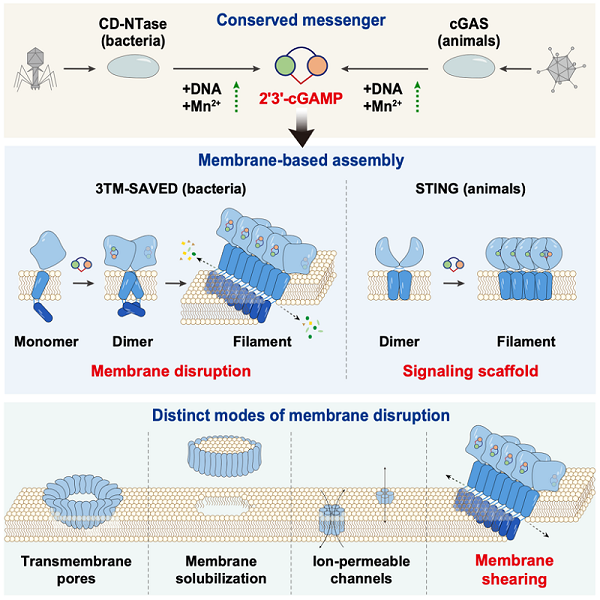
图:2'3'-cGAMP介导的多样性免疫机制
中国科学院生物物理研究所高璞研究员与北京理工大学高昂教授为论文共同通讯作者。生物物理所高艺娜研究员、博士生李肇隆和周昱菲为共同第一作者。此外,生物物理所孙飞研究员/朱赟研究员团队的李伟民博士后、高璞研究员团队的李权锦/石苗/赵春秋/刘松青、高昂教授团队的王靖格/叶枫为研究提供了重要帮助。
文章链接:https://www.cell.com/cell/fulltext/S0092-8674(26)00344-2
(供稿:高璞研究组)
附件下载: