
大脑的“夜间保洁”停摆后,阿尔茨海默病悄悄上门
你是否也经历过这样的夜晚--工作没做完、手机刷不停、思绪乱如麻,最终牺牲睡眠,熬夜到天明?第二天头昏脑涨、记忆断片,安慰自己"周末补一觉就好"。但大脑从不接受"赊账"。最新科学研究表明:每一次强制清醒的深夜,大脑都在进行一场危险的"代谢淤积",这不是疲劳,而是一场针对神经元、静默无声的"慢性投毒",你的每一次熬夜都可能是在为阿尔茨海默病铺路。
大脑的"夜间保洁系统":睡眠如何清洗毒性蛋白
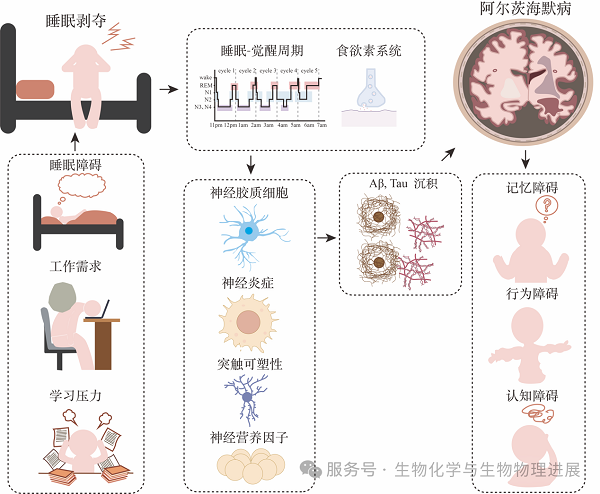
白天,数十亿神经元激烈对话,产生名为β淀粉样蛋白(Aβ)和tau的代谢副产物。这些物质具有神经毒性,若堆积不去,便是阿尔茨海默病脑中标志性斑块与缠结的起点[1]。睡眠,尤其是深度睡眠阶段,是大脑的"夜间保洁时间"。此时,神经胶质细胞收缩,细胞间隙扩大,脑脊液得以洪流般冲刷组织,将日间积存的Aβ、tau等毒性蛋白清运出去[2]。而睡眠剥夺会让这个保洁系统"停摆":动物研究表明,睡眠剥夺会导致小鼠脑内Aβ积累速度加快,突触结构受损,认知功能下降[3]。临床研究表明,哪怕只有一个夜晚不睡觉,健康成人大脑中Aβ的沉积就会显著增加[4]。长期如此,蛋白质逐渐聚集形成斑块和缠结,侵蚀神经元,最终导致记忆衰退、认知障碍。
恶性循环:睡眠与阿尔茨海默病的"死亡螺旋"
睡眠不足与阿尔茨海默病的关系,不是单向因果,而是一场双向的恶性循环[5]。
睡眠→疾病:Aβ/tau清除受阻→炎症激活→神经细胞受损→记忆功能下降,病理进程加速。
疾病→睡眠:斑块/缠结干扰睡眠调节中枢→失眠、睡眠片段化、昼夜节律紊乱。
这意味着睡眠不仅是阿尔茨海默病的"受害者",更是其"推动者"。保护好睡眠,就是在为大脑的未来投保。
睡眠不足"腐蚀"大脑的三大隐形杀手
垃圾堆积:Aβ与tau蛋白的"滞留危机"
睡眠剥夺不仅堵塞"清运"通道,更火上浇油地打开了"生产阀门"。它上调β分泌酶(BACE1)的活性,让产生Aβ的"原料切割"环节加速,导致毒性蛋白"产大于销",形成不可逆的淀粉样斑块[6]。
炎症风暴:小胶质细胞的"叛变"
大脑的常驻免疫部队--小胶质细胞,负责吞噬垃圾,但在长期睡眠剥夺下会从"精确清道夫"陷入"狂暴的焦土模式"。它们过度激活,大量释放IL-1β、TNF-α等炎症因子。这些因子本为清除威胁,但在持续刺激下,却转为攻击健康的神经元突触,并营造一个持续低度发炎的脑内环境,这恰恰是神经元退行性变的最佳温床[7]。
突触损伤:记忆连接的"断线"
睡眠是记忆巩固的关键期,突触是记忆的物理载体。睡眠剥夺会直接降低突触后密度蛋白95(PSD95)的表达,抑制长时程增强(LTP)效应--这是记忆巩固的细胞基础[8]。其结果不仅是记性变差,更是突触结构的物理性丢失。睡眠不足会削弱突触可塑性,影响神经元连接强度,导致学习困难、记忆模糊。长期如此,突触结构受损,认知功能加速下滑。在阿尔茨海默病早期,这种由睡眠问题引发的突触损伤,可能远早于大规模神经元死亡,成为认知坍塌的第一块多米诺骨牌。
打破循环:重塑大脑"睡眠防线"的四大策略
首先,生活方式干预是改善睡眠、保护大脑的基础。核心在于校准生物钟,重建稳定的昼夜节律[9]。这可以通过几个关键行为来实现:第一,每天固定起床时间,这比固定入睡时间更为重要;第二,早晨接触阳光至少30分钟,以有效抑制夜间残留的褪黑素,让大脑快速清醒;第三,夜间主动避免蓝光暴露,以促进褪黑素的自然分泌,为入睡做好准备。
其次,针对特定的神经调控系统进行干预,可直接作用于"清醒开关"。大脑中负责维持清醒的食欲素(下丘脑分泌素)系统是关键靶点[10]。目前,食欲素受体拮抗剂类药物已被批准用于治疗失眠,其原理正是精准地"沉默"那些在夜间过度活跃、驱使人保持清醒的神经元。前沿研究正在进一步探索,这类药物能否在阿尔茨海默病的高危人群中,通过有效改善睡眠质量来延缓其大脑病理进程。
再者,通过代谢干预为大脑创造修复环境同样至关重要。这主要包括两种方式:一是采用生酮饮食,这种饮食模式能够提升脑内具有保护作用的因子水平,从而促进神经元的自我修复;二是坚持规律运动,它可以直接、有效地提升脑源性神经营养因子(BDNF)的水平,这种因子被誉为"大脑的肥料",能显著增强神经细胞的生存能力并加强它们之间的连接[11-12]。
最后,新兴的科技手段为睡眠干预提供了新的可能性。 诸如非侵入性的光生物调节(如特定波长的红光/近红外光照射)和经颅磁刺激等神经调控技术,目前正处于积极探索阶段[13]。这些技术旨在通过物理方式直接调节大脑的睡眠-觉醒周期,未来有望成为一种非药物的、用于干预阿尔茨海默病等神经退行性疾病的新途径。
结语:写给每一个夜不能寐的你
因此,睡眠不是一个可选项,而是神经代谢的必需环节。当你关灯躺下,你并非在休息,而是在启动一套精密的、维持大脑长期健康的生理防御程序。每一次熬夜,都在透支认知资本;每一夜安眠,都在为大脑储蓄未来。如果你经常失眠、睡眠浅、白天困倦--这不仅是疲劳问题,更是大脑发出的早期警报。对抗阿尔茨海默病,或许没有特效药,但拥有每一个深度的夜晚,就是我们每个人都能执行的、最基础的脑神经保护性治疗。今晚,就让我们从放下手机、调暗灯光开始,给大脑一个真正的"夜间保洁"。好好睡觉,是最简单、最温暖的自我保护。(详情请点击阅读原文)
参考文献
[1] Delic V, Ratliff W A, Citron B A. Sleep deprivation, a link between post-traumatic stress disorder and Alzheimer's disease. J Alzheimers Dis, 2021, 79(4): 1443-1449
[2] Benedict C, Blennow K, Zetterberg H, et al. Effects of acute sleep loss on diurnal plasma dynamics of CNS health biomarkers in young men. Neurology, 2020, 94(11): e1181-e1189
[3] Liao F, Zhang T J, Mahan T E, et al. Effects of growth hormone-releasing hormone on sleep and brain interstitial fluid amyloid-β in an APP transgenic mouse model. Brain Behav Immun, 2015, 47: 163-171
[4] Fauria K, Minguillon C, Knezevic I, et al. Exploring cognitive and biological correlates of sleep quality and their potential links with Alzheimer's disease (ALFASleep project): protocol for an observational study. BMJ Open, 2022, 12(12): e067159
[5] Wheelock M D, Strain J F, Mansfield P, et al. Brain network decoupling with increased serum neurofilament and reduced cognitive function in Alzheimer's disease. Brain, 2023, 146(7): 2928-2943
[6] Chen L, Huang J, Yang L, et al. Sleep deprivation accelerates the progression of Alzheimer's disease by influencing Aβ-related metabolism. Neurosci Lett, 2017, 650: 146-152
[7] McGeer E G, McGeer P L. Neuroinflammation in Alzheimer's disease and mild cognitive impairment: a field in its infancy. J Alzheimers Dis, 2010, 19(1): 355-361
[8] Wang C, Gao W R, Yin J, et al. Chronic sleep deprivation exacerbates cognitive and synaptic plasticity impairments in APP/PS1 transgenic mice. Behav Brain Res, 2021, 412: 113400
[9] Yin C, Zhang M, Cheng L, et al. Melatonin modulates TLR4/MyD88/NF-κB signaling pathway to ameliorate cognitive impairment in sleep-deprived rats. Front Pharmacol, 2024, 15: 1430599
[10] Zhou M, Li Y. Effect of different doses of almorexant on learning and memory in 8-month-old APP/PS1 (AD) mice. Peptides, 2023, 167: 171044
[11] Yang Y, Wang X, Xiao A, et al. Ketogenic diet prevents chronic sleep deprivation-induced Alzheimer's disease by inhibiting iron dyshomeostasis and promoting repair via Sirt1/Nrf2 pathway. Front Aging Neurosci, 2022, 14: 998292
[12] Zhao Y, Dai Q, Li Y, et al. Exercise therapy in the application of sleep disorders. Front Neurol, 2024, 15: 1324112
[13] Yang L, Wu C, Parker E, et al. Non-invasive photobiomodulation treatment in an Alzheimer Disease-like transgenic rat model. Theranostics, 2022, 12(5): 2205-2231
作者简介
严思茹:北京联合大学生物化学工程学院硕士生,研究方向为食品营养学。
蔡明扬:北京联合大学生物化学工程学院硕士生,研究方向为食品营养学。
戴雪伶:北京联合大学生物化学工程学院教师。研究方向:阿尔茨海默病机理研究及生物活性物质功效评价。
(作者:严思茹、蔡明扬、戴雪伶)
(本文来源于公众号:生物化学与生物物理进展)
附件下载: