
中科院和北京大学合作在人神经胶质母细胞瘤的
2015年12月3日,中科院生物物理所刘光慧实验室同北京大学汤富酬实验室及中科院动物研究所曲静实验室合作,在《Nature communications》杂志发表了题为“PTEN deficiency reprogrammes human neural stem cells towards a glioblastoma stem cell-like phenotype”的研究论文。该研究揭示了人神经干细胞中的基因突变是形成神经胶质母细胞瘤(GBM)的源驱动力,为实现针对携带特定基因突变的神经胶质母细胞瘤的精准治疗提供了新型研究平台和药物评价体系。
神经胶质母细胞瘤是原发性脑肿瘤中最常见且致死率最高的恶性肿瘤,该类肿瘤在术后及放化疗后极易复发,这导致患者的中位生存期通常不超过16个月。胶质瘤干细胞(GSC)是存在于神经胶质母细胞瘤中的一种具有强致瘤性的细胞类群,通常认为胶质瘤干细胞介导了神经胶质母细胞瘤的细胞异质性、耐药性和预后不良。以往基于小鼠的研究提示了神经干细胞或神经前体细胞可能是胶质瘤干细胞的源头细胞类型,但由于缺乏合适的人类研究体系,该假说在人类转化医学中一直无法得到直接验证。因此,目前针对于神经胶质母细胞瘤的精准治疗尚缺乏明确有效的细胞和分子靶标。
考虑到衰老是神经胶质母细胞瘤患病的重要风险因素,因此研究团队假设衰老所伴随的基因组不稳定性(基因突变率的增加)可能是人类神经干细胞发生恶性转化的分子诱因。抑癌基因PTEN的功能失活是神经胶质母细胞瘤中最常见的遗传改变之一,该遗传突变通常伴随神经胶质母细胞瘤侵袭性增强和对药物抵抗的增加,因此该研究直接聚焦于PTEN缺失是否会驱动人神经干细胞发生恶性转化。研究人员首先利用TALEN介导的基因编辑技术实现了人胚胎干细胞中PTEN基因的纯合性敲除。这些经过基因编辑的人胚胎干细胞进一步被定向诱导分化为神经干细胞和间充质干细胞。研究结果显示,靶向敲除PTEN基因选择性诱发人神经干细胞发生致瘤性转化,而间充质干细胞则表现为加速衰老。PTEN缺失的神经干细胞表现出肿瘤相关的代谢和基因表达谱改变,且获得了在免疫缺陷小鼠颅内形成肿瘤的能力。另一个抑癌基因p53的缺乏可明显增强PTEN缺失的神经干细胞的致瘤性。PTEN在神经干细胞中定位于细胞核中,并且结合在PAX7基因的启动子区与CREB/CBP相互作用,抑制PAX7的转录。PAX7在PTEN缺失后的上调,介导了神经干细胞的致瘤性转化,也增加了胶质瘤干细胞的侵袭性。研究也发现,PAX7与PTEN的表达水平在胶质瘤临床大数据库中呈现负相关性,进一步确证了PTEN-PAX7通路在神经胶质母细胞瘤发病过程中的关键作用。最后,研究者通过对临床上已使用的抗肿瘤药物库进行评价时发现,丝裂霉素C(Mitomycin C)能够选择性诱导PTEN缺失的神经干细胞发生凋亡,提示了未来用于针对PTEN突变型神经胶质母细胞瘤精准治疗的一种可能方案。至此,研究人员发现了PTEN保护人神经干细胞的一种新机制,并建立了新型的人类神经干细胞研究平台,以便系统精确地分析各类促使人神经干细胞发生恶性转化的因素。该项研究有望为神经胶质母细胞瘤的精准治疗提供新的靶点和思路。
该工作由中科院生物物理所、北京大学、中科院动物所以及北京脑重大疾病研究院等科研机构合作完成。中科院生物物理所刘光慧研究员、北京大学汤富酬研究员及中科院动物所曲静研究员为该论文的共同通讯作者。中科院生物物理所段顺磊和袁国红以及北京大学刘晓萌为本文的并列第一作者。研究受到科技部973计划、863计划,国家自然科学基金,北京市自然科学基金,以及中科院干细胞与再生医学战略先导专项等资助。
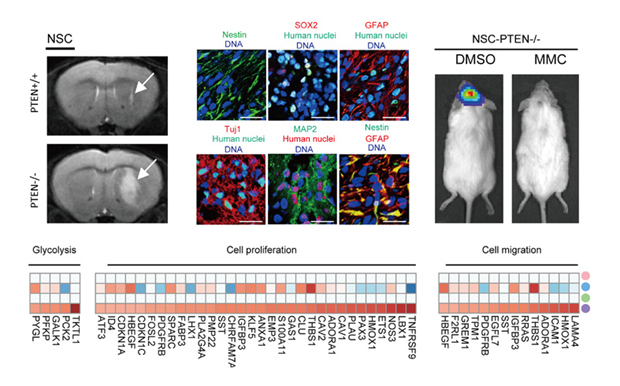
图:PTEN缺失的人神经干细胞能在免疫缺陷小鼠颅内形成神经胶质母细胞瘤样的肿瘤,该肿瘤可被丝裂霉素C特异性杀伤(Duan et al. Nat Commun 2015. 10.1038/NCOMMS10068)。
(供稿:刘光慧课题组)
附件下载: