
为生物组织的介电功能特性拍张高清照片
在生物医学影像的世界里,"看清结构"与"读懂功能"始终是两大核心追求。传统超声成像能精细勾勒组织形态,却难以揭示其内在功能特性;新兴的微波热声成像能反映组织的介电属性,但在分辨细微结构上仍面临挑战。能否有一种技术,真正实现"既见森林,又见树木",这正是微波热声与超声双模态显微成像技术致力实现的突破--不仅是两种成像方式的简单叠加,更是力求在微观尺度上实现结构与介电功能信息深度融合的新范式。
生物医学影像从"单打独斗"走向"协同作战"
生物医学影像技术发展至今,已形成多种模态并存的格局。超声成像凭借其无辐射、实时、成本较低等优势,成为临床诊断中不可或缺的"眼睛"[1],其对比度主要来源于组织间的声阻抗差异,对功能信息的捕捉能力有限。微波热声成像则通过脉冲微波激励组织产生超声信号,反映组织的介电特性,在功能成像方面表现出独特优势[2],已逐步应用于关节疾病和乳腺肿瘤等领域的检测研究[3-4]。然而,单一模态往往只能提供片面的信息。在脑科学、骨代谢疾病和肿瘤早期诊断等前沿领域,研究者不仅需要看清组织结构的细微变化,更希望了解这些变化背后的功能状态。因此,多模态融合成像成为生物医学影像发展的重要趋势,即通过整合不同成像机制的优势,构建更全面、更立体的生物组织信息图谱[5]。

双模态成像从"宏观层析"迈向"微观显微"
早期的微波热声/超声双模态研究多集中于层析成像,分辨率通常在亚毫米级别,虽能实现一定程度的形态与功能结合,却难以满足更细微层次的观测需求[6-7]。要实现真正的"显微"级别成像,必须克服两大核心瓶颈。
分辨率限制:传统微波热声成像受微波脉冲宽度等制约,成像分辨率大多在0.5 mm以上;而高频超声显微成像虽分辨率高,却难以与微波热声层析成像系统兼容。
信息融合困难:简单的图像叠加无法实现真正的信息互补,两种图像需在空间上精准配准、在信息层面深度融合,这对探头设计、信号同步与重建算法都提出了高要求。
近年来,随着高频超声换能器、短脉冲微波源与先进图像重建算法的发展,双模态成像开始向显微尺度突破。来自南佛罗里达大学和重庆邮电大学的联合团队提出采用70 ns短微波脉冲激励与25MHz高频点聚焦超声换能器探测方案,结合信号层面的融合重建策略首次实现了百微米级的三维双模态超声热声显微成像,为在细微层次同时获取组织结构与介电特性信息奠定了技术基础。(详情请点击阅读原文)
从"看见"到"看懂",赋能精准医学研究
这项技术的突破,其意义不止于分辨率的提升,更在于它为生命科学研究和临床诊断提供了不可替代的信息融合视角。
为脑科学研究提供新工具:在脑切片成像中,双模态系统不仅能清晰显示皮层、海马、胼胝体等精细结构,还能通过以组织介电特性差异为对比度基础的微波热声信号强度差异区分灰质与白质,助力神经环路研究与脑疾病机制探索。
助力骨骼疾病早期诊断:在骨质疏松模型中,双模态成像不仅可观察骨组织结构变化,还能同步获取骨组织的介电特性信息,从结构与功能双重维度评估骨质量,为骨骼发病机制研究与早期诊断提供新型敏感标志物。
走向智能化、集成化与临床化
尽管当前系统仍处于实验室阶段,但其展现出的潜力已为未来发展方向勾勒出清晰路径。
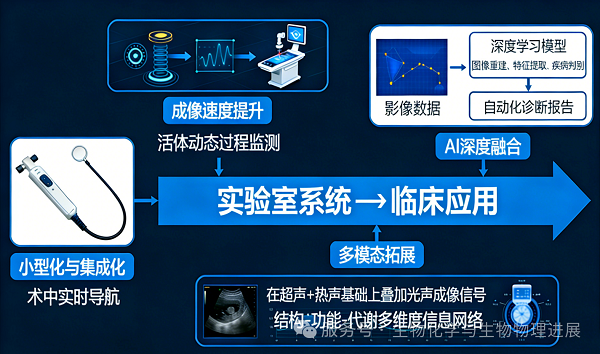
设备小型化与集成化:未来可发展紧凑型手持式双模态探头,甚至与内镜技术结合,实现术中实时导航与病理边界判定。
成像速度与实时性提升:通过扫描机制优化、重建算法优化,有望实现动态过程监测,应用于活体研究。
与人工智能深度融合:结合深度学习进行图像重建、特征提取与疾病判别,实现自动化分析与诊断,提升结果的客观性与可重复性。
拓展多模态融合维度:未来可进一步融合光学、光声等成像模式,构建"结构-功能-代谢"多维度信息网络,更全面解析生命活动与疾病过程。
结 语
从单一模态到多模态融合,从宏观层析到微观显微,生物医学影像技术的发展始终围绕着"更清晰、更深入、更全面"的目标推进。微波热声与超声双模态显微成像的出现,正是旨在细微层次上推动结构与功能一体化观测的重要一步。
它不仅是一项技术创新,更提供了一种整合性的新研究视角。让我们同时获取"解剖形态"与"介电功能"信息。随着技术不断成熟与临床前验证的深入,双模态显微成像有望成为精准医学和转化研究中一项重要的显微分析平台,协助研究人员更全面、更动态地理解生命的微观过程。
参考文献
[1] Orosz G, Szabó R Z, Ungi T, et al. Lung ultrasound imaging and image processing with artificial intelligence methods for bedside diagnostic examinations. Acta Polytech Hung, 2023, 20(8): 69-87
[2] Liu Q, Chao W, Wen R, et al. Optimized excitation in microwave-induced thermoacoustic imaging for artifact suppression. IEEE Trans Med Imaging, 2025, 44(1): 436-446
[3] Wan P, Liu S, Tian R, et al. Compressive sensing combined deep learning for fast microwave-induced thermoacoustic tomography. J Appl Phys, 2023, 133(10): 104502
[4] Qiang T, Wang Y, Lu X, et al. Multi-scale rapid microwave-induced thermoacoustic imaging system for multi-joint detection. In 2024 IEEE International Conference on Computational Electromagnetics (ICCEM). Nanjing, China, 2024: 1-3
[5] Kim C, Chen Z. Multimodal photoacoustic imaging: systems, applications, and agents. Biomed Eng Lett, 2018, 8(2): 137-138
[6] Tan Q, Ji Z, Xing D. Quantitative measurement of polar-molecule perfusion for tumor detection by thermoacoustic Doppler ultrasound dual-modality imaging. Phys Rev Appl, 2019, 11(6): 064006
[7] Wang X, Huang L, Chi Z, et al. Integrated thermoacoustic and ultrasound imaging based on the combination of a hollow concave transducer array and a linear transducer array. Phys Med Biol, 2021, 66(11): 115011
作者简介
聂银强:重庆邮电大学电子科学与工程学院硕士生,研究方向:生物医学微波热声成像。
迟子惠:重庆邮电大学集成电路学院副教授,研究方向:生物医学微波热声成像。
蒋华北:南佛罗里达大学教授,研究方向:光学/光声/微波热声成像技术、影像导引神经调控/靶向基因疗法/癌症手术、转化医学及高性能医疗器械产业化。
(作者:聂银强、迟子惠、蒋华北)
(本文来源于公众号:生物化学与生物物理进展)
附件下载: