
陈畅研究组与施松涛团队合作揭示
硫化氢介导的蛋白硫巯化修饰调节免疫稳态机制
硫化氢(H2S)是机体第三类气体信号分子,对机体骨稳态和免疫稳态具有重要的作用。细胞凋亡过程中,可释放一类特殊的细胞外囊泡,称之为凋亡囊泡,其具有良好的免疫调节和促再生作用,而凋亡缺陷会导致严重的自身免疫性疾病、衰老和肿瘤等。但目前对于细胞凋亡和硫化氢气体之间的内在相互联系尚未见报道。2023年12月18日,中国科学院生物物理研究所陈畅团队和中山大学附属口腔医院施松涛团队在Cell Metabolism发表题为 "Apoptosis releases hydrogen sulfide to inhibit Th17 cell differentiation"的研究论文,提出"凋亡产气"新概念:细胞凋亡是机体硫化氢的重要来源,细胞凋亡来源的硫化氢可以通过硫巯化修饰关键蛋白从而抑制Th17细胞异常分化;并首次提出"凋亡传承"新形式:凋亡囊泡能够传承细胞产硫化氢的能力,且该能力与凋亡囊泡治疗红斑狼疮疾病的疗效相关。
该研究利用细胞凋亡缺陷的MRL/lpr和Bim-/-小鼠模型发现:细胞凋亡缺陷引起机体多器官硫化氢水平的降低,后者与Th17细胞异常分化造成的器官炎症性损伤相关。化学性凋亡诱导可上调硫化氢水平,抑制Th17细胞分化并缓解凋亡缺陷小鼠的炎性损伤,从而证实细胞凋亡是机体硫化氢气体的重要来源。机制上,通过硫巯基化修饰的定量蛋白组学筛选出硫化氢作用Th17细胞的关键靶点硒蛋白15(Selenoprotein F,Sep15)以及其修饰位点C38。利用位点突变技术构建Sep15C38A T细胞,发现硫化氢抑制Sep15C38A Th17细胞分化的作用减弱。这表明,Sep15C38是硫化氢抑制Th17分化的关键靶点和位点。进一步通过Co-IP和磷酸化修饰蛋白检测发现,Sep15通过调控STAT1/STAT3蛋白的磷酸化和入核,从而发挥抑制Th17细胞分化的作用(图1)。另外,该研究进一步验证了细胞凋亡具有传承作用,即干细胞来源的凋亡囊泡中具有自主产生硫化氢的作用,且该作用与其治疗红斑狼疮的效果密切相关。
综上,该研究表明细胞凋亡是机体硫化氢稳态的重要来源,并且筛选出Th17细胞上关键的硫化氢作用蛋白Sep15,同时提出凋亡囊泡产生硫化氢从而发挥调控免疫稳态作用的新机制。以"落红不是无情物,化作春泥更护花"为喻意的艺术图片(图2)被选为Cell Metabolism杂志2024年第一期的封面。
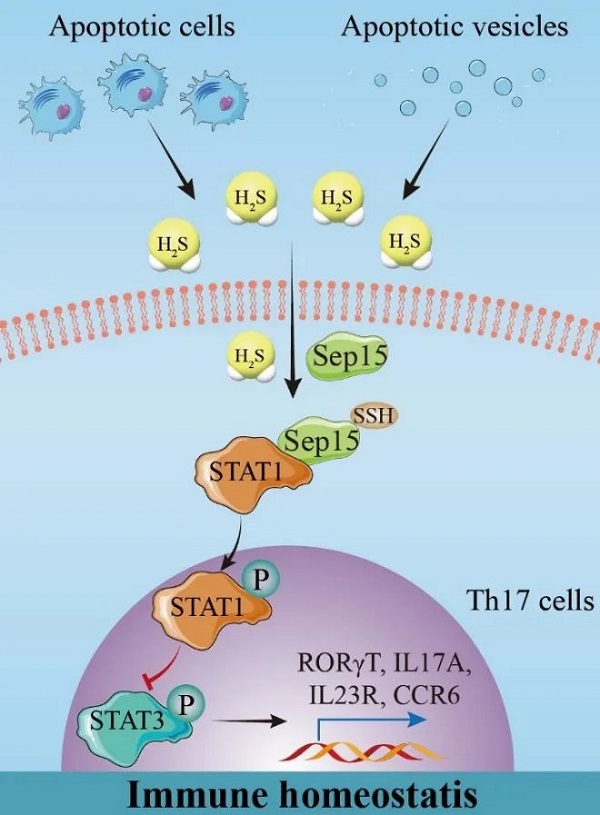
图1. 硫化氢通过Sep15/STAT1/STAT3轴抑制Th17细胞分化

图2. "落红不是无情物,化作春泥更护花"
中山大学附属口腔医院施松涛教授、中国科学院生物物理研究所陈畅研究员为本文通讯作者,中山大学附属口腔医院欧乾民博士后、中国科学院生物物理研究所乔新华副研究员、中山大学附属口腔医院李政诗博士生为本文共同第一作者。国家蛋白质科学中心杨靖研究员和付玲副研究员在蛋白修饰组学研究中给予了大力支持。该项工作得到国家重点研发计划、"珠江人才"创新团队项目、中国科学院战略性先导科技专项项目(B类)和国家自然科学基金的支持。
原文链接:https://doi.org/10.1016/j.cmet.2023.11.012
(供稿:陈畅研究组)
附件下载: