
邓红雨课题组与合作者揭示VMP1和TMEM41B是β冠状病毒侵染过程中DMV形成的关键宿主因子
β冠状病毒家族属于正义单链RNA病毒,包括SARS-CoV-2、SARS-CoV和MERS-CoV等。β冠状病毒侵入宿主细胞后,其基因组RNA借助宿主的翻译系统翻译成两条多蛋白链ORF1a和ORF1b,进而被切割成16个成熟的非结构蛋白nsp1-16。部分nsp蛋白可以引起宿主细胞内膜系统的重塑,形成病毒复制细胞器(replication organelle, RO),其中最主要的RO是双层膜囊泡(double-membrane vesicle, DMV)。病毒复制转录复合体隐藏于RO中进行工作,保护新生成的RNA链免于被宿主细胞识别及清除。但是DMV形成的分子机制和调控机理以及是否有宿主因子参与这一过程均不清楚。
2022年5月11日,中国科学院生物物理研究所邓红雨课题组联合南方科技大学生命科学学院赵燕课题组在《Journal of Cell Biology》上发表了题为"VMP1 and TMEM41B are essential for DMV formation during β-coronavirus infection"的研究论文,揭示了内质网定位的自噬蛋白VMP1和TMEM41B是β冠状病毒侵染过程中必需的宿主因子,并在DMV形成的不同步骤发挥重要作用。
内质网定位的VMP1和TMEM41B是自噬和脂质代谢过程的关键蛋白。近期报道的全基因组CRISPR/Cas9筛选发现VMP1和TMEM41B在SARS-CoV-2的侵染过程中也发挥了重要功能,但具体机理不明。研究人员首先利用同属β冠状病毒家族的小鼠肝炎病毒(mouse hepatitis virus, 可在BSL-2操作)感染细胞实验,证实了VMP1或TMEM41B缺失后,病毒可以入侵细胞,但是无法正常复制,电镜观察也检测不到DMV,提示VMP1和TMEM41B为DMV形成所必需。
之前研究发现,哺乳动物细胞中外源表达的β-冠状病毒蛋白nsp3和nsp4可以通过相互作用引起内质网腔狭窄化,并进一步弯曲形成DMV样双层膜囊泡,为研究DMV形成机制提供了良好的模型。研究人员证实了表达SARS-CoV-2的nsp3和nsp4也可以诱导DMV形成,并且通过荧光蛋白酶保护实验(fluorescence protease protection, FPP)发现nsp3位于DMV的外膜上,而nsp4位于DMV内膜上,且这种分布对于DMV形成必不可少。利用nsp3和nsp4诱导DMV形成这一模型,研究人员发现TMEM41B敲除细胞中, nsp3和nsp4的结合显著减少,而过表达TMEM41B可以促进nsp3和nsp4的结合。VMP1缺失不影响nsp3和nsp4的相互作用和内质网的狭窄化,但是狭窄的内质网形成同心圆样结构,而非正常的DMV。这些结果说明VMP1和TMEM41B在DMV形成的不同阶段发挥功能。
研究人员在线虫中进行全基因组RNAi筛选发现,敲低磷脂酰丝氨酸(phosphatidylserine, PS)的合成酶基因pssy-1可以抑制epg-3(VMP1的线虫同源基因)突变引起的线虫表皮细胞中脂滴的增大。在哺乳动物细胞中敲降pssy-1的同源基因PTDSS1也可以抑制VMP1敲除引起的脂滴增大,并可以部分逆转其DMV异常的表型。过去研究发现VMP1具有磷脂翻转酶(scramblase)功能,结合本研究结果,提示PS可能在DMV的形成中发挥了关键作用。
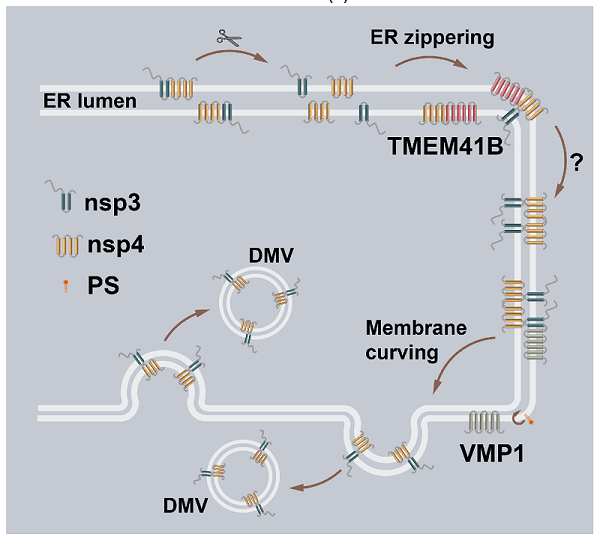
图. VMP1和TMEM41B在DMV形成不同阶段发挥功能的示意图
综上所述,该研究表明SARS-CoV-2的非结构蛋白nsp3和nsp4分别位于DMV膜的两侧,这一独特的分布对于狭窄的内质网弯曲形成DMV囊泡非常重要。内质网自噬蛋白VMP1和TMEM41B在DMV生成的不同步骤发挥关键作用,而PS累积可能是VMP1 敲除细胞中多种膜结构缺陷的重要原因。这些发现揭示了冠状病毒复制过程中宿主因子协同病毒蛋白调控内膜系统重塑的分子机制。
南方科技大学生命科学学院赵燕助理教授和中国科学院生物物理研究所邓红雨研究员为本论文通讯作者,中科院生物物理所博士后季明明、南方科技大学博士研究生李萌和中科院生物物理研究所博士研究生孙龙为并列第一作者。本研究得到了科技部国家重点研发计划、国家自然科学基金委、中国科学院以及深港脑科学创新研究院等项目的支持。
该项工作发表后,很快获得《Autophagy》期刊主编Dr. Dan Klionsky的关注,并邀请作者就该工作为期刊专栏"Autophagic Puncta"撰写评述。2022年7月28日,题为"DMV biogenesis during β-coronavirus infection requires autophagy proteins VMP1 and TMEM41B"的 Punctum发表。
文章链接:
https://www.tandfonline.com/doi/full/10.1080/15548627.2022.2103783
(供稿:邓红雨研究组)
附件下载: