
杨鹏远课题组建立基于我国C2亚型代表株的HBV复制细胞工具
乙肝病毒(Hepatitis B Virus, HBV)感染易导致慢性乙型肝炎、肝纤维化、肝硬化和肝细胞癌等,严重损害患者生命健康,造成沉重的经济和社会负担。全球约有2.57亿慢性乙肝感染者,其中大约三分之一在中国。
2022年2月24日,中科院生物物理研究所杨鹏远课题组在《Parmacological Research》杂志发表题为"Establishment of an inducible cell line for Hepatitis B virus genotype C2 and its pharmacological responses to interferons"的研究论文,构建了针对我国高发的C2亚型HBV细胞模型,填补了C基因型HBV机制研究及其药物筛选稳定细胞工具的缺乏。
HBV进化过程中由于基因组突变累积形成9个基因型(A型到I型)和1个准基因型(J型),各基因型又包含多种亚型。研究人员基于对NCBI数据库中我国提交的HBV全基因组序列统计,发现65.2%的毒株为C型,其中C2亚型占大多数。根据相关临床报道,C型HBV比A型和D型易导致慢性感染和肝纤维化,致癌能力强,且对干扰素等药物响应差;其中,C2亚型HBV在青少年患者中表现出更高程度的肝炎、肝纤维化和肝损伤。但是,目前实验室常用HBV复制细胞工具均基于欧美国家流行的D型HBV构建,尚缺乏针对我国高发与肝病密切的C基因型HBV稳定复制的细胞模型。
研究人员对1449条分离自我国的HBV全基因组公开序列进行分析,综合考虑基因型、血清型、特征性突变位点等信息,选出17.3株作为我国C2亚型HBV的代表性基因组序列,利用tet-off诱导表达系统将包含前基因组序列的1.05× HBV整合入HepG2细胞,筛选建立了HepG2-17.3细胞系。该细胞系稳定表达分泌HBsAg抗原,诱导后表达分泌HBeAg抗原,利用C2亚型preS1 N端特异序列检测分泌的HBV DNA滴度在3×105 copies/mL,并且验证了rcDNA-cccDNA的复制循环。在评价HepG2-17.3细胞系对临床一线药物的响应情况中发现I型干扰素和II型干扰素联用比单用可获得更好的抗病毒效果,且干扰素处理后ISG分子(已报道可发挥抗HBV作用)激活情况与D型HBV复制细胞显著不同。因此,HepG2-17.3细胞的建立为针对我国高发的C2亚型HBV基因型特点进行病毒机制及治疗药物研究提供了有力工具。
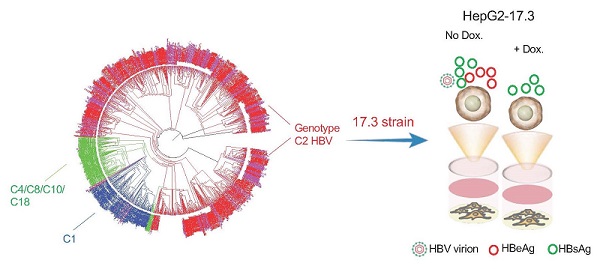
图1. 可诱导C2型HBV稳定细胞株的构建流程图。
中国科学院生物物理所杨鹏远研究员为本文通讯作者。杨鹏远组姜韶东博士,王欣博士为本文共同第一作者。该研究得到中国科学院和国家自然科学基金委的经费支持。
文章链接:https://doi.org/10.1016/j.phrs.2022.106142
(供稿:杨鹏远研究组)
附件下载: