
杨鹏远/季雄课题组揭示乙肝病毒DNA与人基因组互作景观图
乙型肝炎病毒(hepatitis B virus, HBV)感染是全球性重大公共卫生健康问题之一。全球目前乙肝病毒慢性感染者约2.6亿人,每年接近100万人死于慢性乙肝导致的肝功能衰竭、肝硬化和肝细胞癌。HBV属嗜肝DNA病毒科,在人体肝脏细胞核内可以形成cccDNA和整合入人体基因组等病毒DNA形式稳定存在,这是HBV维持长期慢性感染的关键,因此研究乙肝病毒与宿主基因组相互作用特征具有重要意义。
2020年12月29日,中科院生物物理所杨鹏远课题组与北京大学生命科学学院季雄课题组合作在《Cell Discovery》杂志发表了题为" 3D landscape of Hepatitis B virus interactions with human chromatins "的研究成果。系统的阐述了乙肝病毒cccDNA和整合形式的HBV DNA与宿主基因组相互作用的特征,为HBV感染及相关疾病治疗提供了新的潜在靶点。
该研究采用3C-HTGTS(3C-high-throughput genome-wide sequencing)技术在HBV感染HepG2-NTCP细胞中发现HBV cccDNA与宿主基因组的相互作用倾向于富含H3K4me3、H3K9ac、H3K4me1和H3K27ac等组蛋白修饰的活跃增强子(Enhancer)和启动子(Promoter)。更为重要的是,在稳定表达HBV的HepAD38细胞中发现,整合形式的HBV DNA能够和宿主基因组DNA形成染色质环(chromatin loop)结构,并且倾向于和宿主基因的启动区域互作。
研究人员发现,HBV cccDNA与宿主基因组中富含H3K4me1区域相互作用,进而通过染色质免疫共沉淀(ChIP-qPCR)发现,HBV cccDNA上确实存在丰富的组蛋白H3K4me1修饰。当敲低细胞内的介导组蛋白H3K4me1发生的赖氨酸特异性甲基转移酶2C/D(KMT2C/D)时,HBV RNA转录显著下调,上清中分泌的HBV表面抗原(HBsAg)和E抗原(HBeAg)含量显著降低,结果提示HBV cccDNA可通过宿主甲基转移酶介导病毒的转录调控。该研究成果拓展了HBV在人体细胞核中分布特征的认知,还为治疗HBV感染及相关疾病提供了新的潜在靶点。
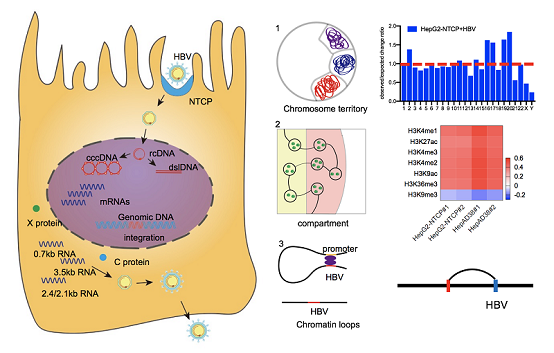
图1. 乙肝病毒与宿主基因组相互作用景观特征示意图。
该工作由中国科学院生物物理研究所、北京大学和北京协和医院多家单位合作完成。生物物理研究所中科院感染与免疫重点实验室杨鹏远研究员和北京大学生命科学学院季雄研究员为本文的共同通讯作者,中国科学院生物物理研究所博士生杨博和北京大学生命科学学院博士生李伯源为本文共同第一作者。该研究得到科技部、国家自然科学基金委和中科院的经费支持。感谢李文辉、黄爱龙、李国红、胡家志和张治华等的大力支持,感谢生物物理所及感染免疫科研平台提供的帮助。
文章链接:https://www.nature.com/articles/s41421-020-00218-1
(供稿:杨鹏远研究组)
附件下载: