
朱冰课题组发现TNF-α介导的炎症响应记忆现象并阐述其分子机理
2020年11月6日,《eLife》杂志在线发表了中国科学院生物物理研究所生物大分子国家重点实验室朱冰课题组的最新研究成果:"Sustained TNF-α stimulation leads to transcriptional memory that greatly enhances signal sensitivity and robustness"。这项工作发现炎症因子TNF-α的持续刺激能够诱导部分炎症响应基因产生转录记忆,对后续的TNF-α刺激产生更快、更强、更灵敏的响应。该现象的分子机制核心为信号诱导的转录因子激活及其诱发的DNA主动去甲基化。
信号分子能激活特定基因以调控生物学过程。大多数基因对信号分子的初次刺激和二次刺激的反应是相同的。但是,少数基因在接受信号分子的二次刺激时,会有更快、更强的反应,这种现象叫做转录记忆。促炎症因子TNF-α可以激活NF-κB等信号通路,在慢性炎症的发病中发挥了关键作用。拮抗TNF-α是风湿性关节炎和溃疡性结肠炎等慢性炎症的重要治疗手段。
在炎症反应中至关重要的促炎症因子TNF-α可否介导转录记忆?如果能,具体的机制是什么?在哺乳动物中,哪种表观遗传学修饰可以在转录记忆的形成中起决定性作用?哪些因素决定了被信号分子激活的基因是否具有转录记忆?解决这些问题将有助于对慢性炎症和转录记忆的认识。
通过对插入在HEK293F细胞被DNA甲基化沉默的报告基因的研究,发现持续性TNF-α刺激能够诱导转录记忆,使报告基因在接受二次TNF-α刺激时发生更快、更强的激活。随后,若干具有对TNF-α刺激具有转录记忆效应的内源基因被发现。其中转录记忆效应最强的内源基因是编码偏头痛治疗靶点CGRP的CALCB基因。
转录因子NF-κB结合区域的去甲基化现象伴随着转录记忆的建立。敲除具有DNA去甲基化功能的TET基因后,全部对TNF-α具有转录记忆效应的基因都失去了转录记忆。这表明,主动DNA去甲基化在转录记忆的建立过程中具有不可取代的作用。
然而,并非所有NF-κB的靶基因都具有转录记忆,因为只有在NF-κB结合位点附近有着较高的DNA甲基化程度和CpG位点密度的位点才能成为具有记忆潜能的转录调控元件。
有趣的是,少数具有转录记忆效应的基因(例如CACLB基因),能够在接受低于初始TNF-α刺激浓度100倍的二次刺激时,仍能发生显著更强的表达激活。这表明,一旦转录记忆被确立,细胞在接受后续炎症刺激时响应灵敏度会大幅上升,这一现象可能有助于解释急性炎症向慢性炎症的转换。
总结而言,该工作发现了促炎症因子TNF-α介导的依赖于NF-κB信号通路和DNA主动去甲基化的转录记忆效应。这种转录记忆效应,使具有转录记忆的基因对后续TNF-α刺激发生更快、更强、更敏感的响应。这一转录记忆形成的机制预期广泛存在于其它信号系统,该工作为此类研究提供了研究流程的模板。
本研究在中国科学院生物物理研究所完成。朱冰研究员为通讯作者,赵作栋博士和张珠强研究员为共同第一作者。朱冰课题组的李晶晶博士研究生、董强博士、熊俊博士、李颖峰博士和兰孟颖博士研究生等对本工作有重要的贡献。澳门大学的李刚教授在研究过程中给予了大力协助。本研究得到了国家自然科学基金委、科技部和中国科学院的资助。
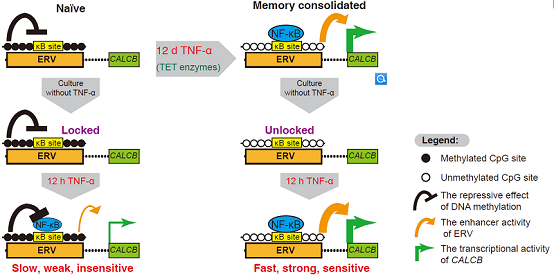
图1: TNF-α刺激介导转录记忆形成的分子机理(以CALCB基因为例)
文章链接:https://elifesciences.org/articles/61965
(供稿:朱冰研究组)
附件下载: