2024年8月5日,中国科学院生物物理研究所朱平研究组和李国红研究组合作,在《Cell Research》杂志在线发表了题为“Structural basis for linker histone H5–nucleosome binding and chromatin fiber compaction”的研究论文。该研究获得了由连接组蛋白H5折叠十二个核小体形成的染色质颗粒3.6埃(Å)分辨率的冷冻电子显微镜结构,首次报道了由全长连接组蛋白H5(包括其N端结构域和C端结构域)及其与核小体核心颗粒(nucleosome core particle,NCP)形成的完整染色质小体(chromatasome)结构,并建立了由连接组蛋白H5介导形成的30nm染色质纤维的全原子结构模型。
在真核生物中,基因组DNA被分层包装到细胞核内不同层次的染色质组织中。其中,DNA缠绕在核心组蛋白组成的八聚体上组成核小体,多个核小体组成的串珠状结构在连接组蛋白等的帮助下折叠形成直径在30nm左右的染色质纤维,并进一步折叠形成更为紧密的染色质高维结构。在这个过程中,30nm染色质纤维承上启下,连接核小体串珠和高维染色质结构,其折叠规律和调控机制是理解染色质结构的关键,对于阐明染色质在调节基因表达和其他DNA依赖性活动中的生物学作用具有重要意义。
此前,朱平研究组和李国红研究组合作,解析了由连接组蛋白H1.4介导的重组30nm染色质纤维分辨率为11埃(Å)的冷冻电镜结构(Song et al,Science 2014)。在本研究中,研究者通过长期努力,解析了由12×177bp_601DNA、核心组蛋白(H2A、H2B、H3和H4)和连接组蛋白H5组装形成的H5结合十二核小体的染色质(以下称为H5-染色质纤维)的分辨率为3.6Å的冷冻电镜结构(图1)。
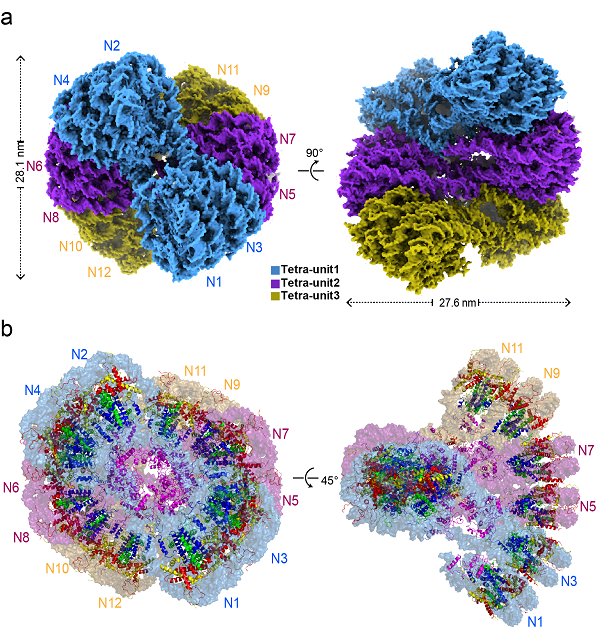
图1 H5-30nm染色质纤维冷冻电镜结构(a)及原子结构模型(b)
研究者发现,与H1.4-30nm染色质纤维类似,H5-30nm染色质纤维以4个核小体为一个结构单元,各单元之间通过相互扭曲折叠Zig-Zag形成一个和DNA右手双螺旋类似的左手双螺旋高级结构(图1a)。本研究获得的H5-30nm染色质结构解析分辨率(3.6Å)比研究组前期发表的H1.4-30nm染色质结构解析分辨率(11Å)有了突破性的提升,研究者关心的染色质高级结构形成过程中的关键相互作用,如四核小体结构单元内部以及单元之间的核心组蛋白-核心组蛋白、核心组蛋白-连接组蛋白、以及连接组蛋白-linker DNA之间的相互作用细节得以清晰呈现。基于本研究获得的高分辨率冷冻电子显微密度图,研究者建立了H5-30nm染色质纤维一个完整的全原子结构模型(图1b)。
连接组蛋白在染色质压缩以及高级结构形成中起着关键作用。不同的连接组蛋白均包括一个N端结构域(NTD),一个球形结构域(globular domain, GD)以及一个C端结构域(CTD)。由于富含带电氨基酸,连接组蛋白的NTD和CTD在溶液状态下呈现高度无序的状态。迄今为止只有占全长连接组蛋白的1/3左右的GD结构域的结构得到解析。在本研究中,研究者获得了连接组蛋白H5的全长蛋白,包括其N端结构域NTD和C端结构域CTD的原子分辨率结构,第一次建立了一个完整染色质小体(chromosome,即核小体核心颗粒NCP+全长连接组蛋白)的原子分辨率结构(图2)。研究者发现,在H5-30nm染色质纤维中,连接组蛋白H5以非对称三点接触方式结合在核小体核心颗粒上,其中H5的CTD结构域形成一种经典的HMG-like螺旋折叠方式紧密结合在linker DNA上,并通过H5的NTD和CTD结构域与连接DNA的相互作用促进染色质高级结构的折叠和高级结构形成。
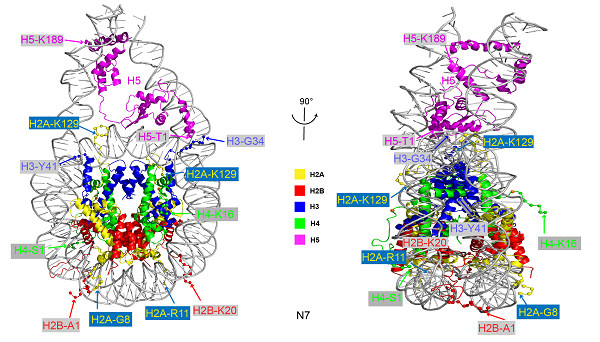
图2 全长连接组蛋白H5与核小体核心颗粒形成的完整染色质小体结构
研究者发现,染色质纤维高级结构形成过程中具有多重结构不对称性。同时,研究者还利用一系列遗传学、基因组学和生物物理方法系统验证了真核生物芽殖酵母中四核小体折叠单元的生理功能和结构特征。基于以上结果,研究者提出了连接组蛋白H5介导的核小体结合和染色质折叠和高级结构形成的分子机制模型(图3)。
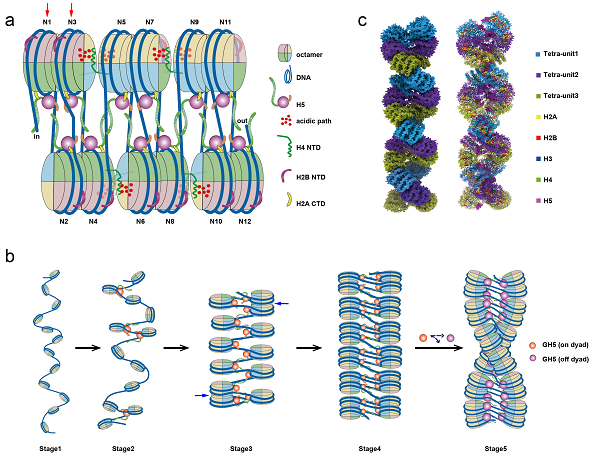
图3 连接组蛋白介导的30nm染色质纤维折叠及高级结构组装模型
本研究结果对于染色质纤维高分辨率结构精细模型的建立,以及染色质的高级结构组装和表观遗传调控机制的研究具有重要意义,为理解体内染色质结构建立的分子基础和各种表观遗传因素对染色质结构调控的可能机理提供了重要的结构基础。
中国科学院生物物理研究所朱平研究组博士生李文艳、李国红研究组博士生胡杰、武汉大学生命学院副教授宋峰(朱平研究组毕业博士生)、李国红研究组副研究员于娟为论文的共同第一作者;朱平研究员和李国红研究员为共同通讯作者。生物物理研究所李伟,中国科学院分子细胞科学卓越创新中心周金秋等团队提供了重要帮助。该研究获得科技部、国家自然科学基金委以及中国科学院等项目的资助。
文章链接:https://www.nature.com/articles/s41422-024-01009-z
(供稿:朱平研究组)
 附件下载:
附件下载: