2022年2月10日,中科院生物物理研究所朱冰课题组与许瑞明课题组合作,在《Science》杂志在线发表题为"Highly enriched BEND3 prevents the premature activation of bivalent genes during differentiation"的研究论文,报道了CpG岛结合蛋白BEND3在二价基因上的高度富集,可以防止这些基因在分化过程中过早激活。
CpG岛是脊椎动物基因组上的重要调控序列,富含非甲基化的CpG二核苷酸,常出现在活跃的管家基因(housekeeping genes)以及发育相关的二价基因(bivalent genes)的启动子区域。2021年,瑞士弗里德里希·米歇尔生物医学研究所Dirk Schübeler课题组发现,序列特异性转录因子 BANP能够结合并激活一部分含有CpG岛启动子的必需基因的表达。而同样含有CpG岛启动子的二价基因,是否也会受到序列特异性结合蛋白的调控并不清楚。由于目前关于CpG岛结合蛋白的研究还很有限,关于CpG岛基因的表达调控还有很多尚待研究。朱冰课题组2016年发表在《Molecular Cell》上的论文曾鉴定到BEND3在体外倾向于结合含有非甲基化修饰的DNA,但关于该蛋白在体内的生理功能知之甚少。
在这项研究中,研究人员发现BEND3能够特异性结合在基因组中含有CpG岛的活跃基因和二价基因的启动子区域,并找到了BEND3特异性结合的DNA基序。通过和许瑞明组合作,研究人员解析了最关键的第四个BEN结构域结合DNA基序的共结晶结构,为BEND3序列特异性和DNA甲基化敏感结合特性提供了结构依据。利用小鼠模型,他们发现Bend3敲除的小鼠胚胎会在原肠胚形成阶段死亡。通过体内畸胎瘤形成实验和体外分化实验,研究人员证明了Bend3敲除的小鼠胚胎干细胞虽然能够保持自我更新,但却丧失了分化的能力。为了找到发育和分化缺陷的分子机制,研究人员利用体外类胚体分化(EB分化)实验,结合RNA-seq 技术,发现数百个被BEND3高度占据的二价基因在分化早期被异常激活。结合各种全基因组学分析,研究人员发现Bend3敲除会导致一部分富含BEND3的二价基因启动子上SUZ12和H3K27me3水平的下降,导致这些失去了PRC2和H3K27me3保护的二价基因在分化过程中在不恰当的时间被错误地提前激活,最终导致发育和分化的失败。
在胚胎干细胞中,二价启动子(bivalent promoter),即同时存在激活性的H3K4me3和抑制性的H3K27me3组蛋白标记,通常被认为将发育相关基因维持在"蓄势待发"的状态,以备在分化时快速激活。然而在小鼠胚胎干细胞中敲除MLL2以擦除H3K4me3修饰后,这些发育基因的快速激活并没有受到影响。这项研究工作证明了二价启动子上的H3K27me3修饰的重要性,H3K27me3在分化前期起到"手刹"的作用, 帮助这些基因维持在"戒急缓发"的状态,防止组织特异性基因的过早激活,保障胚胎发育过程中基因时空特异性地表达。
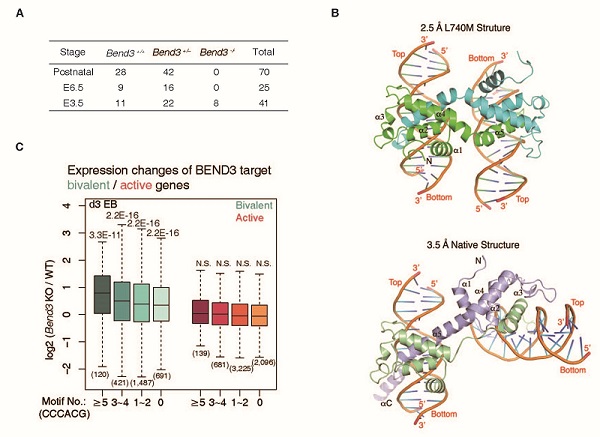
图: BEND3在小鼠胚胎发育以及胚胎干细胞分化过程中发挥重要功能
中科院生物物理所朱冰研究员和许瑞明研究员为本文的共同通讯作者。朱冰课题组张晶博士,张彦博士和许瑞明课题组游庆龙博士为本文共同第一作者。该研究得到科技部、国家自然科学基金委和中国科学院的支持。
文章链接:https://www.science.org/doi/10.1126/science.abm0730
(供稿:朱冰研究组)
 附件下载:
附件下载: