皮肤作为我们人体最大的器官,集物理防护、体温调节、免疫调节等多重功能于一身。皮肤虽然强大,但也会受伤。无论是日常的擦伤、割伤,还是严重的烧伤、放射伤等,都会破坏皮肤的完整性,影响其功能。尤其是糖尿病、烧伤或放射性创面,会让伤口环境变得特别复杂,创面的修复需要进行人工干预。
伤口敷料是目前临床实践中公认的治疗方法。然而,传统敷料纱布、 棉球、绷带抑菌性差,黏附性弱,机械性能差,容易诱发炎症、阻碍血管生成,并且需要频繁更换新敷料,无法为伤口愈合提供一个有利的环境[1]。自组装水凝胶由小分子化合物、生物大分子、高分子化合物及肽类化合物等物质通过非共价或共价相互作用自发组织或聚集形成。
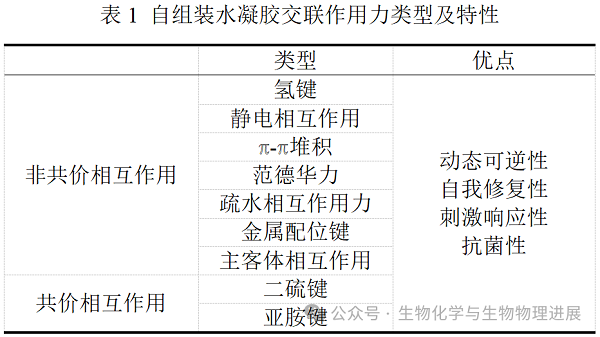
物理优势
水凝胶本身具备疏松多孔的三维网格结构,与细胞外基质(extracellular matrix,ECM)类似,向海绵一样具有优异的吸水能力和锁水能力。同时,自组装水凝胶特殊的交联机制,让其获得动态可逆性、自修复能力和刺激响应性的"超能力"。因而,自组装水凝胶能更好地为受损皮肤提供保护,避免或控制伤口感染,提供合适的愈合环境,促进伤口愈合,更接近于理想敷料[2]。
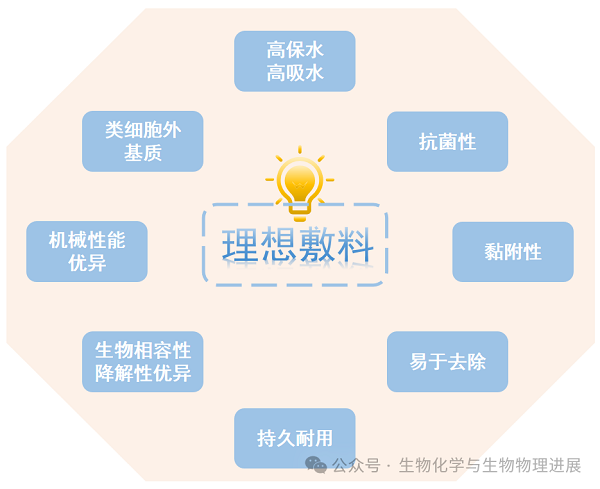
理想敷料特点
功能优势
促进细胞增殖:自组装水凝胶通过其独特的亲水三维网络结构,为细胞提供了一个接近生物体内自然环境的三维培养环境。这种环境为细胞模拟在生物体内存活的条件,保持细胞间的相互作用,并促进更逼真的生化和生理反应[3]。
促进止血凝血:水凝胶疏松多孔的海绵状网络,可以吸引聚集红细胞和血小板[4],加速形成血凝块,可以实现快速止血。除此之外,含醛基、氨基、羟基等官能团的水凝胶[5],会像"钩子"一样紧密地黏附于皮肤表面,共同形成物理止血屏障。
加速愈合:感染、炎症和氧化应激是形成慢性创面的三大"元凶",并且相互影响。自组装水凝胶的合成原料和(或)负载物质带来的制胜法宝-抗菌[6]、抗炎[7]、抗氧化能力[8],可以改善伤口皮肤创面的微环境,加快伤口愈合。
调节再生:肉芽增生、血管再生、胶原蛋白沉积是创面愈合再生的关键。自组装水凝胶就像是伤口的"超级助手",对再生通路进行调节[9],促进细胞增殖和迁移,诱导血管内皮生长因子(vascular endothelial growth factor,VEGF)、表皮生长因子(epidermal growth factor,EGF)、碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)等合成,减少ECM 和生长因子降解[10],从而确保创面正常增生和成熟。
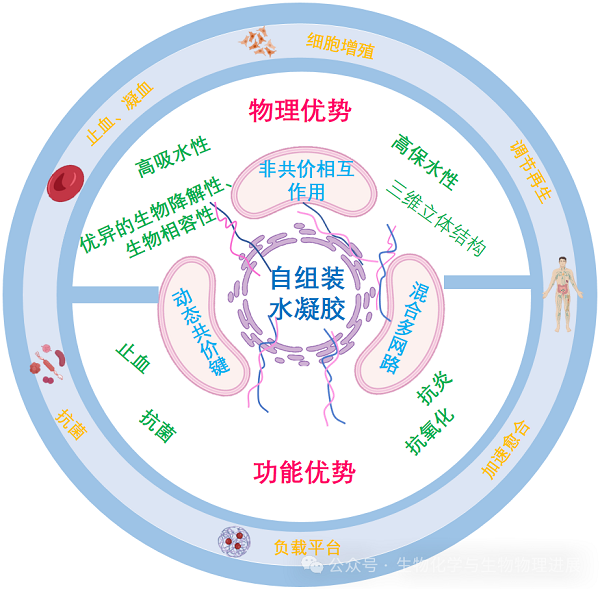
自组装水凝胶的优势及作用
小结与展望
传统敷料仅实现了"敷"的效果,然而自组装水凝胶可以同时满足"敷"和"料"的作用效果。并且自组装水凝胶仍在不断地优化改进,更契合于理想敷料的要求,更好地应对皮肤伤口复杂的愈合过程。(详情请点击阅读原文)
未来自组装水凝胶应趋向于:
从天然可自组装的生物分子多肽、脂质、蛋白质和多糖出发,构建多策略联用的仿生凝胶;
改善原材料的性能和交联方式,提升水凝胶储存能力,延长水凝胶使用寿命和(或)形成可循环利用;
对于水凝胶尚未明确的交联过程进一步研究和探明,实现凝胶降解速率的可控;
应用3D打印和三维显微成像技术,设计构建一对一专用的凝胶敷料;同时考虑时间因素,利用计算机仿真技术模拟愈合进程,从而形成完美契合理想敷料的自组装水凝胶。
参考文献
[1] Ovington L G. Advances in wound dressings. Clin Dermatol,2007,25(1):33-38
[2] Yildirimer L,Thanh N T K,Seifalian A M. Skin regeneration scaffolds: a multimodal bottom-up approach. Trends Biotechnol,2012,30(12):638-648
[3] Schneider A,Garlick J A,Egles C. Self-assembling peptide nanofiber scaffolds accelerate wound healing. PLoS One,2008,3(1):e1410
[4] Zhang H,Xu Y,Lei Y,et al. Tourmaline nanoparticles modifying hemostatic property of chitosan/polyvinyl alcohol hydrogels. Mater Lett,2022,324: 132718
[5] You S,Huang Y,Mao R,et al. Together is better: poly(tannic acid) nanorods functionalized polysaccharide hydrogels for diabetic wound healing. Ind Crops Prod,2022,186: 115273
[6] Santhini E,Parthasarathy R,Shalini M,et al. Bio inspired growth factor loaded self assembling peptide nano hydrogel for chronic wound healing. Int J Biol Macromol,2022,197: 77-87
[7] Zhao Y,Liu X,Peng X,et al. A poloxamer/hyaluronic acid/chitosan-based thermosensitive hydrogel that releases dihydromyricetin to promote wound healing. Int J Biol Macromol,2022,216: 475-486
[8] Zhang B,Lv Y,Yu C,et al. Au-Pt nanozyme-based multifunctional hydrogel dressing for diabetic wound healing. Biomater Adv,2022,137: 212869
[9] Jafari H,Alimoradi H,Delporte C,et al. An injectable,self-healing,3D printable,double network co-enzymatically crosslinked hydrogel using marine poly- and oligo-saccharides for wound healing application. Appl Mater Today,2022,29: 101581
[10] Pérez-Rafael S,Ivanova K,Stefanov I,et al. Nanoparticle-driven self-assembling injectable hydrogels provide a multi-factorial approach for chronic wound treatment. Acta Biomater,2021,134: 131-143
作者简介
李 超:中国辐射防护研究院放射医学与环境医学所研究实习员,主要从事合成生物学及辐射损伤救治方向的研究。
郭玉凤:中国辐射防护研究院放射医学与环境医学所助理研究员,主要从事合成生物学及辐射损伤救治方向的研究。
党旭红:中国辐射防护研究院放射医学与环境医学所研究员,主要从事辐射生物效应及辐射损伤救治方向的研究。
(作者:李超、郭玉凤、党旭红)
(本文来源于公众号:生物化学与生物物理进展)
 附件下载:
附件下载: