人类对生物组织、器官电活动的关注和研究长达数个世纪。早在十八世纪中叶,意大利著名的生理学家Galvani通过金属导线将避雷针与蛙腿神经-肌肉实验标本的坐骨神经相连,发现随雷电的出现蛙腿肌肉发生抽动;此外,他将一侧蛙腿的坐骨神经切断,与对侧蛙腿肌肉完整的坐骨神经表面相接触,断离的坐骨神经受到电刺激时亦可引起对侧蛙腿肌肉的收缩。Galvani由此得出结论,肌肉收缩需要"动物电"的传导[1]。1831年,Matteucci[2]使用电流计(galvanometer,以Galvani命名)直接测定到了损伤电流蛙腿神经和肌肉断端,并首次利用受损蛙肌产生的损伤电位显示了神经、肌肉动作电位的存在。
后来的研究逐渐发现,内源性电信号广泛存在于生物体个体发育、组织再生及伤口修复的过程。以角膜伤口为例,研究发现,当外界因素导致皮肤出现伤口时,会使致密上皮细胞形成的屏障受到损伤,由于上皮细胞缺失使跨上皮电位发生短路,完整上皮结构继续正常定向运输带电离子与水平创伤处形成电势差,进而构成完整的闭合回路,导致从完整上皮基底侧流向伤口的电流出现,并在整个皮肤损伤过程中维持较长时间的稳定电场[3]。随着伤口愈合,以及上皮屏障的逐渐修复,跨上皮电位也恢复成初始状态,内源性电场逐渐消失。在组织和器官上均覆有上表皮,伤口的产生破坏了上皮细胞间的屏障,使得伤口处的电势下降,并低于远离创口处未受伤上皮细胞的电势。由此产生的电势差驱动电流向电势较低的区域(即创口处)流动,这样便产生了横向的、指向创口中心的电场(图1)。
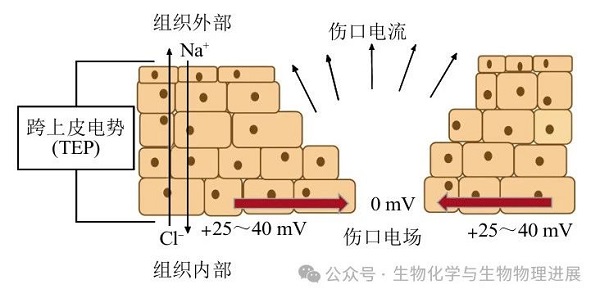
伤口电场产生的原理[4]
伤口愈合是一个复杂的动态生理过程,在伤口愈合的不同阶段,存在受到一系列受到严格调控的生物学过程,其中包括成纤维细胞、角质形成细胞和其他类型的细胞协调增殖和迁移,重塑肉芽组织,进而恢复皮肤组织的上皮层结构。影响伤口愈合的因素有很多,研究发现,创伤处产生的内源性电场是指导上皮角质细胞定向迁移的重要信号,此外,电场能指导人类永生化表皮细胞的定向迁移(详情请点击阅读全文),电场也能促进皮肤成纤维细胞的增殖和迁移,增加生长因子的分泌,以及促进成纤维细胞分化为肌成纤维细胞,从而促进伤口愈合[5]。更为重要的是,当其他引导信号同时存在时,生理强度的电信号是指导细胞定向迁移的主导信号[6],通过激动剂或抑制剂调控内源性电场的大小会显著影响伤口的愈合过程[7-8]。此外,使用外加电场刺激哺乳动物伤口愈合的临床试验显示,在外加电场的作用下伤口愈合率从13%显著提高到50%[9]。
迅速有效的伤口愈合一直是医疗领域一个持久且具有挑战性的话题。随着糖尿病和老龄化人口的不断扩大,慢性或不愈合的伤口也给人类带来了越来越多的健康问题和经济负担。应用电场促进伤口愈合无疑促进伤口愈合提供了一种新颖有效的途径和方法。自上世纪中叶以来,从治疗角度出发的电刺激促进伤口愈合已广泛报道。体外和体内研究为临床试验铺平了道路,将电刺激确立为一种可接受的治疗方法。尽管电刺激在促进伤口愈合方面的效果被广泛传播,但电刺激尚未被接受为一种既定的治疗模式。其中研究成果之间缺乏趋同性是原因之一。另外在电场刺激伤口愈合的过程中会产生一些次要效应,其中一个突出的次要影响是组织损伤。采取哪些措施使电场在发挥促进伤口愈合作用的同时尽量减少组织的损伤,是推动电刺激应用于伤口愈合治疗过程中需解决的重要问题。
参考文献
[1] Piccolino M. The bicentennial of the Voltaic battery (1800-2000): the artificial electric organ. Trends Neurosci, 2000, 23(4): 147-151
[2] du Bois-Reymond E. Vorlaufiger Abriss einer Untersuchung über den sogenannten Froschstrom und über die elektromotorischen Fische. Ann Der Phys, 1843, 134(1): 1-30
[3] Zhao M. Electrical fields in wound healing-An overriding signal that directs cell migration. Semin Cell Dev Biol, 2009, 20(6): 674-682
[4] 董晓蒙, 高晶, 孙沁, 等. 内源性电场及其生物学意义. 生物化学与生物物理进展, 2016, 43(8): 731-738
[5] Rouabhia M, Park H, Meng S, et al. Electrical stimulation promotes wound healing by enhancing dermal fibroblast activity and promoting myofibroblast transdifferentiation. PLoS One, 2013, 8(8): e71660
[6] Zhao M, Song B, Pu J, et al. Electrical signals control wound healing through phosphatidylinositol-3-OH kinase-gamma and PTEN. Nature, 2006, 442(7101): 457-460
[7] Song B, Zhao M, Forrester J V, et al. Electrical cues regulate the orientation and frequency of cell division and the rate of wound healing in vivo. Proc Natl Acad Sci USA, 2002, 99(21): 13577-13582
[8] Song B, Zhao M, Forrester J, et al. Nerve regeneration and wound healing are stimulated and directed by an endogenous electrical field in vivo. J Cell Sci, 2004, 117(Pt 20): 4681-4690
[9] Nuccitelli R. A role for endogenous electric fields in wound healing. In Current Topics in Developmental Biology. Amsterdam: Elsevier, 2003: 1-26
作者简介
张世豪:云南师范大学生命科学学院硕士研究生,从事电场指导细胞定向迁移促进创面愈合的机制研究。
(作者:张世豪)
(本文来源于公众号:生物化学与生物物理进展)
 附件下载:
附件下载: