抑郁症是一种临床症状表现为情绪低落、快感缺失的常见情感障碍类疾病。2020 年全球重度抑郁症患者约为 1.93 亿人。特别是经历新冠疫情后,抑郁症发生率持续攀升[1]。目前指导临床用药的"单胺假说"仍存在一定的缺陷,疾病发生机制不清;临床一线抗抑郁药物的治疗有效率仅为33%,同时还可能出现药物抵抗等副作用[2]。
抑郁症发生的可能新机制
在近几十年中,炎症反应被认为是重度抑郁患者发生的关键原因。同时,外源性甲醛(FA)重复暴露会诱发小鼠出现抑郁样行为,并被认为直接触发了神经炎症。温州医科大学程建华、童志前团队首先提出了外周注射脂多糖(LPS),上调血液中的氨基脲敏感胺氧化酶(semicarbazide-sensitive amine oxidase, SSAO,一种FA生成酶),产生内源性FA并直接刺激免疫细胞释放大量的炎症因子而诱发抑郁的机制假说。(详情请点击阅读原文)
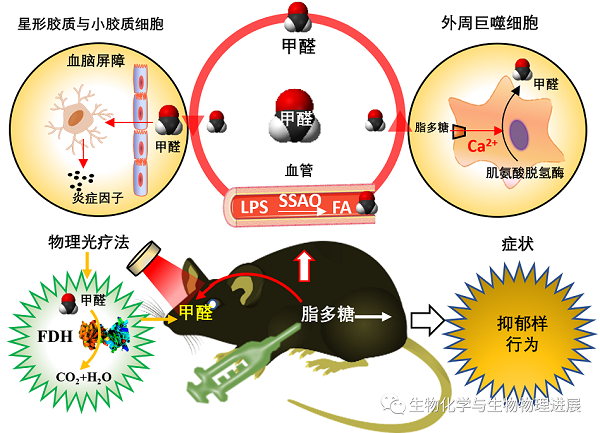
甲醛促发神经炎症诱发抑郁发生的机制
近 20 年来,光生物调节(photobiomodulation, PBM)疗法逐步被用于临床治疗抑郁等心理疾病[3]。如红光(red light, RL)/近外红光(near-infrared,NIR)具有抗炎作用,可减少小鼠抑郁样行为。研究发现,630 nm 红光照射作为一种非侵入性手段,可以有效激活甲醛脱氢酶(formaldehyde dehydrogenase, FDH),并消除小鼠脑中蓄积的FA。基础和临床结果都显示具有良好的穿透性,未发现明显不良反应;是一种潜在的临床治疗抑郁的方法。(详情请点击阅读原文)
PBM在抑郁症等精神疾病中的应用
630 nm 红光照射作为一种新型 PBM 治疗方法已经被用于挽救认知与记忆。下图为温州医科大学程建华、童志前团队自行研发的红光治疗仪。

自行研发的高能红光治疗仪
现有对红光治疗抑郁的研究,主要是其对线粒体电子传递链的末端酶--细胞色素酶 C 的影响。红光可通过提高细胞色素酶 C 的活性,促使 一氧化氮(NO )从双核中心解离,增加线粒体膜电位,进而促进 ATP 的释放,增强神经保护和代谢能力。
程建华、童志前团队主要探索了红光激活FDH,降解FA,减轻神经炎症的通路。实验中,630 nm 红光改善小鼠抑郁样行为的机制主要包括:一是630 nm 红光照射直接激活 FDH及时清除急性上升的 FA;二是630 nm 红光照射激活细胞色素酶 C ,挽救了因内源FA被神经元细胞分解代谢而产生的甲酸盐对细胞色素酶 C 的抑制作用,避免糖酵解持续升高导致的神经细胞毒性。研究发现,630 nm 红光治疗照射1周后即改善小鼠抑郁样行为,因此在抑郁症早期干预中可能更具有重要的临床应用价值。(详情请点击阅读原文)
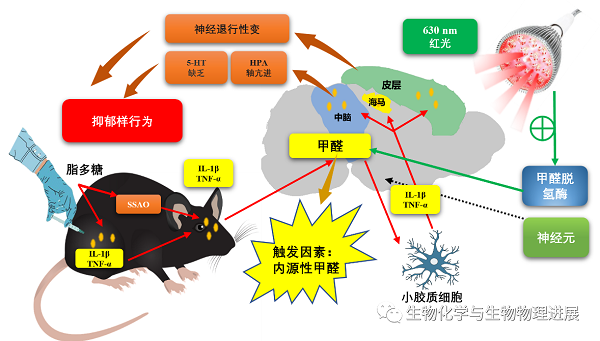
红光治疗抑郁的机制图
临床应用前景
前期研究表明[4],内源性FA是多种精神疾病发生的关键因子,如阿尔茨海默病、抑郁症等。过量蓄积的FA具有神经毒性,并导致Aβ等蛋白质的错误折叠,同时与神经炎症发生、氧化应激等密切相关。
程建华、童志前团队首先证实蓄积的脑内源FA可能是治疗抑郁的新靶点,消除脑内源FA可减轻其产生的一系列神经炎症、氧化应激等反应,630 nm红光是一种有效清除FA蓄积的非侵入性治疗方式,对抑郁具有显著治疗作用。
目前,课题组开发的红光治疗仪已经得到临床验证,对认知障碍等精神疾病患者进行试验,证实血液中FA含量显著下降,显著提高认知水平。纳米红光疗法,作为一种无创物理疗法,有可能成为临床治疗精神类疾病的新策略。
参考文献
[1] Mazza M G, De Lorenzo R, Conte C, et al. Anxiety and depression in COVID-19 survivors: role of inflammatory and clinical predictors. Brain Behav Immun, 2020, 89: 594-600
[2] Peng G J, Tian J S, Gao X X, et al. Research on the pathological mechanism and drug treatment mechanism of depression. Curr Neuropharmacol, 2015, 13(4): 514-523
[3] Salehpour F, Mahmoudi J, Kamari F, et al. Brain photobiomodulation therapy: a narrative Review. Mol Neurobiol, 2018, 55(8): 6601-6636
[4] Yue X, Mei Y, Zhang Y, et al. New insight into Alzheimer's disease: light reverses Abeta-obstructed interstitial fluid flow and ameliorates memory decline in APP/PS1 mice. Alzheimers Dement (N Y), 2019, 5: 671-684
作者简介
赵丹睿:温州医科大学精神医学学院本科生,研究方向为内源性甲醛与神经免疫、精神疾病研究。
(作者:赵丹睿)
(本文来源于公众号:生物化学与生物物理进展)
 附件下载:
附件下载: