自列文虎克对庞大的微生物世界做出描述以来,微生物一直被视为聋哑者,在复杂的环境中默默生存繁衍而不与周围的伙伴交流。直至20世纪60年代,科学家才揭示了微生物也能够借助特定的信号分子作为其通讯语言,通过交流与邻居间建立紧密的联系。借助这种复杂而精密的交流系统,微生物能够通过"听-想-做"(即"感知周围的信号-翻译所识别的信息-对外部信号做出响应")的过程,快速感应环境变化,并与邻居进行分工合作、资源共享、协同进化等复杂的群体行为,进而提高在环境中的适应能力。
微生物的交流语言
与微生物交流的邻居可能是同种的个体,也可能是异种的成员,甚至是与他们共享生态幅的其他生物有机体,因此,它们之间交流所借助的语言也各有不同。这些语言广泛存在且具有种属差异,包括化学信号、小分子化合物、信息素,以及细胞间的物理接触等,行使着种内、种间和跨界交流的功能,决定着微生物与相邻生物之间互利共生或是竞争的关系。
通常,微生物在生长过程中能够通过分泌某些小分子进行相互交流,这些信号分子聚集在细胞周围,并在达到阈值浓度后调节自身种群密度,激活下游功能基因的表达,表现出生物发光、毒性表达、抗生素产生以及生物膜形成等行为【1】。这类信号被称为"群体感应"(quorum sensing,QS),是微生物较为通用的交流语言。但对于不同的微生物,还有其偏好使用的独特方言,例如革兰氏阴性菌常利用的信号分子是N-酰基高丝氨酸内酯(AHLs)、长链脂肪酸、脂肪酸甲酯以及自诱导物II(AI-2)。AI-2也可被一些革兰氏阳性细菌所使用,但通常它们更喜欢利用修饰或环状的肽,如寡肽(AIP)。而细菌用于种内和种间交流时,还偏向于使用扩散信号因子(DSF)。对于真菌而言,它们常使用的QS信号分子主要为醇类化合物。另外,在种内、种间及跨界交流中,吲哚常常作为信息素,发挥着重要的介导作用。
除QS信号外,微生物间还存在其他交流语言。群体猝灭信号(quorum quenching,QQ)是微生物破坏信号分子以阻碍QS过程的一种策略。据推断,QQ可能是由QS产生者为清除自身QS信号而进化出的自然机制,或者是产QQ生物与QS信号产生者竞争的一种有效手段【2-3】。此外,抗生素在亚抑制浓度下也可以充当种间信号分子,调节微生物群落的平衡【4-5】,而只有在超过阈值浓度时才会发挥抗菌作用。
这些语言使微生物能够通过感知进行交流,但除了这种有距离地交换信号外,微生物还能够以细胞间的直接接触来传递信息。比如由连接相邻细胞的胞间纳米管(intercellular nanotubes)介导的细菌通讯,可以为种内和种间的物质交换搭建交流网络。此外,原核和真核细胞能够分泌一种进化保守的胞外囊泡(extracellular vesicles,EVs),通过多种内吞途径将信息物质输送到宿主细胞,进而介导着微生物与宿主间的紧密交流【6】。
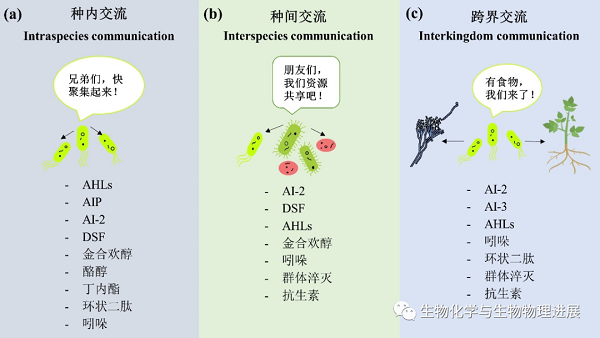
自然界中微生物的主要交流信号
微生物交流的作用
微生物栖居过程中常常需要应对多变的环境,包括资源的匮乏和恶劣条件的刺激。为了获得长久生存,微生物通过交流将单个细胞的功能与群体的需求联系在一起,共同应对外界挑战。通过频繁的信号交流,微生物能够产生生物膜,获得增加抗逆性、抵抗紫外辐射、提高抗生素耐药性等多种生存优势,从而提高了它们在不利条件下繁殖、存活和代谢的几率【7】。另一方面,微生物为了更好地分配资源,通过交流进行生态位分割,实现营养的有效利用,将资源枯竭的可能性降至最低,从而有利于群体的长远发展。最后,微生物借助各种交流与其他物种进行错综复杂的互作,而持续的相互作用驱动了微生物与宿主间的协同进化。
微生物交流的应用
微生物间的交流常常与病原菌的致病性密切相关,通过QS系统调控毒力相关过程,使细菌能避免宿主防御系统对它的早期识别,并在定殖成功后统一种群行为,有效扩大其生态影响。信号交流为微生物带来了生存优势,但同时也成为疾病治疗、农业病害防治及环境修复的新突破口。不同于抗生素,群体猝灭剂控制了病原菌的毒力,抑制生物膜的形成,但不影响细菌的生存生长,因此在减弱致病性的同时,不会造成抗菌治疗的选择压力,是治疗细菌感染性疾病的有效途径【8】。同时,群体感应抑制剂能够有效对抗植物和动物疾病,在农业生产中具有潜在的应用前景。另外,干扰细菌QS系统破坏生物膜,将是未来新型无毒害的生物污损防治手段【9-10】。
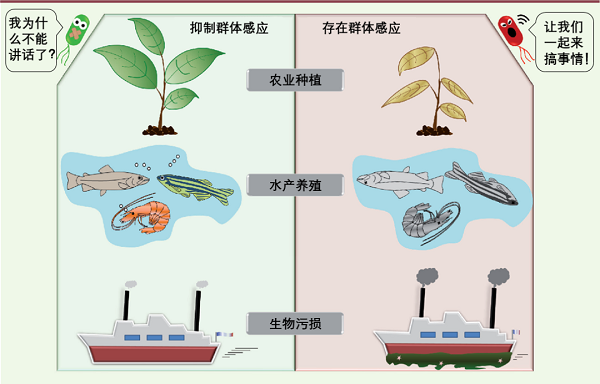
抑制群体感应在限制动植物感染或控制生物污损方面的应用【11】
展望
随着微生物研究的不断深入,人们逐渐认识到生活在庞杂环境中的微生物并不是孤立的存在,而是表现出群体的行为。在群体过程中它们使用多样的交流系统去协调自身活动,感知邻近细胞的动态,并相应调节自身的行为。近年来,更有研究表明,最简单的生命个体--病毒,也在QS信号介导下参与着与宿主间的互作交流【12】。
在过去的几十年里,许多结构和功能多样的信号系统正以惊人的速度被发现,并不断增加着人们对微生物通讯、微生物生理和微生物进化的认知,但是对于许多信号分子的全部面貌和交流分子机制仍存在未知领域。此外,目前对微生物信号的了解大多基于实验室内的纯培养,这对于自然微生物群落而言还只是太仓一粟。因此,未来仍需进行不同生境下多物种交流方式的探索,通过更多新方法来扩充微生物语言库,并借助交流语言去阐释生态事件,解读微生物的行为机制。最后,借助合成生物学对微生物语言进行改造与利用,从而开展更有效的生态修复及病原防控。(详情请点击阅读原文)
参考文献
[1] Kaiser D, Losick R. How and why bacteria talk to each other. Cell, 1993, 73(5): 873-885
[2] Kusari P, Kusari S, Lamsh?ft M, et al. Quorum quenching is an antivirulence strategy employed by endophytic bacteria. Appl Microbiol Biot, 2014, 98(16): 7173-7183
[3] Grandclément C, Tannières M, Moréra S, et al. Quorum quenching: role in nature and applied developments. FEMS Microbiol Rev, 2016, 40(1): 86-116
[4] Liu G, Chater K F, Chandra G, et al. Molecular regulation of antibiotic biosynthesis in Streptomyces. Microbiol Mol Biol R, 2013, 77(1): 112-143
[5] Yim G, Huimi Wang H, Davies Frs J. Antibiotics as signalling molecules. Philos TR Soc B, 2007, 362(1483): 1195-1200
[6] O'donoghue E J, Krachler A M. Mechanisms of outer membrane vesicle entry into host cells. Cell Microbiol, 2016, 18(11): 1508- 1517
[7] Koo H, Yamada K M. Dynamic cell-matrix interactions modulate microbial biofilm and tissue 3D microenvironments. Curr Opin Cell Biol, 2016, 42: 102-112
[8] Suga H, Smith K M. Molecular mechanisms of bacterial quorum sensing as a new drug target. Curr Opin Chem Biol, 2003, 7(5): 586-591
[9] Dobretsov S, Teplitski M, Bayer M, et al. Inhibition of marine biofouling by bacterial quorum sensing inhibitors. Biofouling, 2011, 27(8): 893-905
[10] Dobretsov S, Teplitski M, Paul V. Mini-review: quorum sensing in the marine environment and its relationship to biofouling. Biofouling, 2009, 25(5): 413-427
[11] Mion S, Rémy B, Plener L, et al. Quorum sensing et quorum quenching: Comment bloquer la communication des bactéries pour inhiber leur virulence?. MED SCI, 2019, 35(1): 31-38
[12] León-Félix J, Villica?a C. The impact of quorum sensing on the modulation of phage-host interactions. J Bacteriol, 2021, 203(11): e00687-20
作者简介
程珂珂:清华大学深圳国际研究生院博士后,研究方向为环境微生物的群落与功能,及其与宿主间的互作关系。
(作者:程珂珂)
(本文来源于公众号: 生物化学与生物物理进展)
 附件下载:
附件下载: