
生物物理所杨鹏远课题组揭示
肝癌是第二大癌症,与其他肿瘤相比,肝癌发生的诱因常由于长期的肝脏慢性炎症,如慢性乙型肝炎、非酒精性脂肪肝炎等。在诱导炎症发展成肿瘤的众多因素中,炎性微环境的差异是肝脏炎-癌转化的重要决定性因素。但是,这种炎性微环境如何激活细胞诱导癌变的调控网络和功能机制仍未阐明。
2019年7月29日,Nature Communications杂志在线发表论中科院生物物理所杨鹏远课题组的题为 “ER-residential Nogo-B accelerates NAFLD-associated HCC mediated by metabolic reprogramming of oxLDL lipophagy” 的研究成果。该论文揭示了一种内质网定位蛋白Nogo-B在非酒精性脂肪肝炎向肝癌转化过程中通过调节氧化修饰低密度脂蛋白(oxLDL)代谢重编程促进肝癌的发生发展,阐明了一新的肝脏炎-癌转化机制,为肝癌患者的治疗提供了新的理论基础和防治策略。
肝脏是机体代谢的重要器官,在脂肪代谢中具有重要而独特的作用。代谢紊乱常见于肝癌的发生发展过程中,在中国高发肝病的急、慢性乙肝病毒感染过程中也常伴有代谢调节失常,因此,代谢重编程是肝脏炎症到癌症转化的关键步骤。脂滴代谢是肝脏脂质代谢的重要过程,但它在肝癌进程中的作用研究还很缺乏。如何靶向脂滴动态变化寻找肝癌代谢调节的新机制,对当今社会具有重要的科学意义。
该研究发现,在慢性肝炎的微环境中,LDL被大量氧化为oxLDL,通过CD36大量摄取入肝细胞内,诱导一种内质网定位的蛋白Nogo-B表达上调。 Nogo-B的高表达显著促进了肝癌细胞的生长。在高脂高糖诱导的小鼠肝癌模型中,肝靶向的Nogo-B敲减可以有效地抑制肝癌的发生发展,同时缓解脂肪肝的进程。病理机制研究显示,Nogo-B可以通过与ATG5相互作用促进oxLDL脂滴自噬和降解。有趣的是,这种Nogo-B促进的oxLDL脂滴自噬促进了LPA的大量产生,进而提高Hippo信号通路YAP活性,激活下游癌基因的表达。这种促癌信号的激活在大量的临床数据库分析和肝癌患者的临床样本中得到验证。这些结果证明,CD36-Nogo-B-YAP通路通过调节肝癌细胞重编程,促进病人从肝炎向肝癌的进展,为肝癌肿瘤微环境的研究提供了新思路。
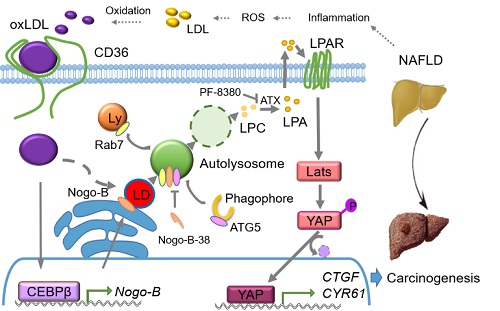
【机制示意图】 Nogo-B促进肝癌细胞代谢重编程的模式图。NAFLD肝炎中的oxLDL摄取入肝细胞促进内质网定位蛋白Nogo-B的表达,促进oxLDL脂滴降解,产生更多的LPA激活YAP,促进了癌基因的表达。
该工作由中国科学院生物物理研究所与香港中文大学医学院、国家消化疾病重点实验室、第二军医大学、国家肝癌中心等多家医学和临床医学中心合作,中国科学院生物物理研究所感染免疫重点实验室杨鹏远研究员和香港中文大学郑诗乐副教授为本文的共同通讯作者,杨鹏远课题组的副研究员田媛和博士生杨彬为本文的共同第一作者。论文感谢来自科技部、国家自然科学基金委和中国科学院的经费支持,感谢中科院生物物理所刘平生课题组、张宏课题组和王晓晨课题组、复旦大学余发星教授和中科院生物物理所和感免实验室科研平台的支持和帮助。
文章链接:https://doi.org/10.1038/s41467-019-11274-x
(供稿:杨鹏远研究组)
附件下载: