黄亿华课题组在细菌脂多糖跨膜转运机理方面取得新进展
2017年4月10日,《Nature Structural & Molecular Biology》在线发表了中国科学院生物物理研究所黄亿华研究员课题组的研究论文 (“Structural basis for lipopolysaccharide extraction by ABC transporter LptB2FG”),解析了一种新型ABC transporter LptB2FG膜蛋白复合体的晶体结构,初步揭示了这种新型ABC transporter从细胞膜上抽提脂多糖(lipopolysaccharide, LPS)分子的分子机制。
LPS又称内毒素,组成革兰氏阴性细菌外膜的外小叶。脂多糖不仅是革兰氏阴性细菌外膜的主要组成成分, 也是导致炎症和人体天然免疫反应的主要原因。一百多年来,科学家们对细菌脂多糖在胞质中的合成已经有了很深入的了解,但直到二十一世纪初,美国普林斯顿大学细菌遗传学家、美国科学院院士Thomas Silhavy 和美国哈佛大学生物化学家Daniel Kahne等发现,细菌脂多糖的跨膜转运以及在外膜上的组装由七个脂多糖转运蛋白(LptA-G)负责完成。其中,LptB, LptF和LptG组成四聚体ABC transporter位于内膜上,负责从内膜外小叶抽提LPS,并通过LptC和LptA将LPS传递给位于外膜上的LptD-LptE复合体,最后完成LPS插膜组装。脂多糖为所有革兰氏阴性细菌生存所必需, 因此对脂多糖分子转运与组装相关蛋白复合体的结构和功能研究不仅可以加深对革兰氏阴性细菌外膜的生成机制的理解,也可以为研发新型抗生素应对日益严峻的革兰氏阴性细菌耐药问题提供解决方案。
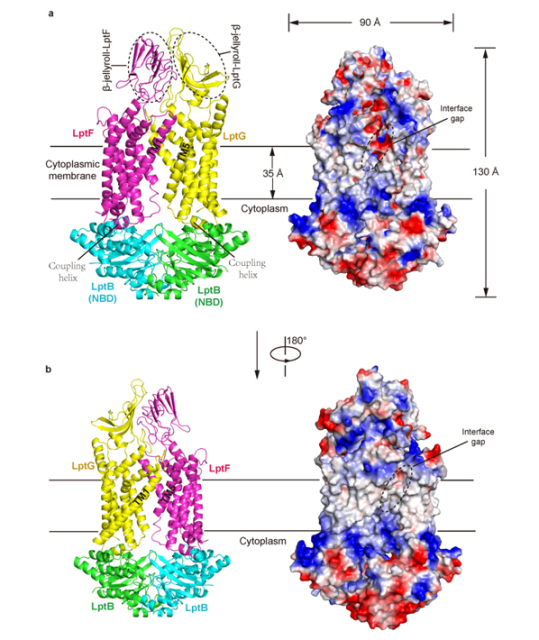
黄亿华研究员课题组在2014年解析了负责脂多糖在细菌外膜上转运和组装的膜蛋白复合体LptD-LptE的2.4埃的高分辨率晶体结构, 初步阐明了脂多糖分子如何进入到细菌的外膜的分子机理(Nature,2014)。经过几年努力,又成功解析了负责从内膜抽提LPS的新型ABC transporter LptB2FG复合体的晶体结构。在LptB2FG复合体中,LptF和LptG各包含一个跨膜结构域(TMD),一个周质侧β-jellyroll结构域和一个与LptB相互作用的α-螺旋。内膜上的LptF和LptG的跨膜结构域形成一个较大的外向开放的“V”型凹槽,结构分析和功能实验初步表明LPS可能从LptF和LptG跨膜结构域的接触面进入“V”型凹槽,在LptB结合和水解ATP提供能量基础上,通过构象变化将LPS转运到β-jellyroll结构域中,完成LPS从内膜的抽提过程。该项研究通过对LptB2FG复合体结构和功能的分析,初步揭示了这种新型的ABC transporter从内膜抽提脂多糖分子的分子机理,并定义LptB2FG为一类Type III ABC exporter与Type I和Type II ABC exporter进行区分。
黄亿华研究员为文章通讯作者,黄亿华课题组博士生骆青山为文章第一作者,生物物理研究所“膜蛋白团队”章新政课题组,上海国家蛋白质科学中心李典范课题组和南京理工大学化工学院周敏课题组也参与了该研究。该研究工作得到了国家杰出青年科学基金,科技部重大研发计划以及中国科学院战略性先导科技专项(B类)的资助。
图示: LptB2FG整体结构
(供稿:黄亿华课题组)
附件下载: