李国红课题组在Developmental Cell上发表研究论文
Developmental Cell期刊于2014年12月31日在线发表了我所李国红课题组研究着丝粒区域染色质特有的细胞周期依赖性装配机制的最新成果,为长期困扰着丝粒生物学领域的CENP-A装配机制问题提供了答案。
着丝粒是一段结构与功能高度特化的染色质区域,在细胞分裂期指导动粒的组装,并在纺锤丝的牵拉下实现姐妹染色单体的分离并向细胞两极移动。CENP-A,作为着丝粒区域染色质的标识分子,是组蛋白H3的变体,可以特异替换着丝粒区域核小体中核心组蛋白H3。CENP-A在着丝粒区域的正确装配对于染色体与基因组的稳定性具有重要的意义。包括组蛋白H3在内的常规组蛋白的表达与装配在时间上趋于一致,通常发生于细胞周期的S期。随着子代DNA的合成,新生成的常规组蛋白随即装配入新生DNA分子,将子代DNA及时地包装成染色质。而CENP-A具有与常规组蛋白截然不同的表达与装配模式,它主要在G2-M期表达,在G1期早期完成着丝粒区域的装配。CENP-A蛋白的表达与其在着丝粒区域染色质的装配这两个过程相互分离又紧密结合,实现这种特殊调控的内在机制成为该领域中一个至关重要的科学问题。
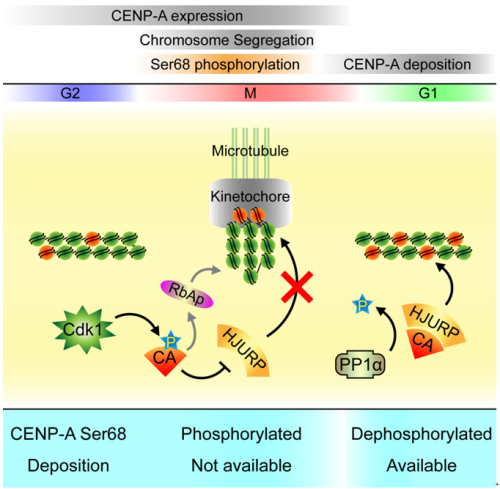
李国红课题组与许瑞明课题组在该领域研究中进行了多年的密切合作,为解决着丝粒生物学领域的这一关键问题做出了一系列具有重要影响力的工作。早在2011年,许瑞明课题组与李国红课题组合作解析了人源CENP-A装配前复合物即CENP-A与其装配因子HJURP复合物的晶体结构,揭示CENP-A分子上的Ser68残基为HJURP识别的关键位点(Hu et al., Genes and Development, 2011)。在此基础上,两个课题组进一步合作,通过一系列生物化学与细胞生物学实验分析,详细地阐述了CENP-A分子上的Ser68可以通过可逆磷酸化修饰来调控HJURP识别与结合的能力。在G2/M期CENP-A蛋白表达后会被Cdk1/CyclinB激酶复合物催化发生Ser68的磷酸化,因此M期CENP-A分子虽然存在,但由于Ser68磷酸化的CENP-A不能被HJURP识别,使得CENP-A不会在M期发生过早的装配。在M期末期,由于Cdk1/CyclinB活性降低,Ser68的磷酸化修饰则被PP1α催化发生去磷酸化,使HJURP可以在这个阶段识别CENP-A并将CENP-A装配入着丝粒区域,从而完成了着丝粒区域染色质在子代细胞中的精确维持。
图例:CENP-A Ser68的可逆磷酸化调控HJURP介导的CENP-A装配机制
本研究工作由李国红课题组的于宙亮与周翔共同完成。同时,本研究工作还得到了我所娄继忠、欧光朔(清华大学)、袁增强等课题组以及武汉大学的张晓东、华东师范大学的翁杰敏、北京蛋白组学研究中心的徐平、和美国贝勒医学院的Shuo Dong等课题组的帮助和支持。该项目得到了科技部、自然科学基金委和科学院的基金支持。
文章链接:http://www.sciencedirect.com/science/article/pii/S1534580714007692
(供稿:李国红课题组)
附件下载: