纳米酶是一类具有类酶催化性能的纳米材料,是新一代人工酶,在生物医学领域有着广泛的应用前景。自2007年首次发现四氧化三铁(Fe3O4)纳米颗粒具有类过氧化物酶活性以来,铁基纳米酶在肿瘤催化治疗和抗菌等方面受到广泛关注。然而,由于铁原子的利用率较低,纳米氧化铁的催化效率往往低于天然酶(如辣根过氧化物酶,HRP)。为了提高铁原子的利用率,人们引入单原子设计用于构筑更加精确的活性位点,通过模拟天然酶的铁卟啉配位结构,显著提高了铁的催化效率和纳米酶的活力。例如,在铁单原子纳米酶中构建诸如FeN4、FeN5或FeN3P等活性位点,其催化效率和动力学可与天然酶相媲美。然而,以铁盐作为铁源与碳氮化物配位,或在金属-有机框架(MOFs)中取代金属,然后再进行热解碳化的合成方法,除了形成单原子铁外,往往还会形成较多的铁团簇或铁单质,并非完全处于单原子状态。这种不可控的铁原子状态不仅影响了纳米酶的类酶活性,也使得精确评估其催化效率变得困难。
为了解决这一问题,高利增研究组提出了一种红细胞模板化策略,以其丰富的血红蛋白作为铁源制备铁单原子纳米酶。其基本理念是改造红细胞内源铁模拟辣根过氧化物酶(HRP)的催化活性中心,由运输氧功能转化为催化功能。每个红细胞含有约2.6亿个血红蛋白,每个血红蛋白含有4个包含铁原子的环状血红素,这使它们成为单原子铁的理想来源,用以制备模拟HRP活性的纳米酶。
为了证明该假设,研究者将细胞固定、盐化和热解碳化等过程相结合,以红细胞作为模板,合成了具有均匀单原子Fe的纳米酶。如图1所示,这种红细胞模板纳米酶(Erythrocyte-templated nanozymes,ETN)表现出类过氧化物酶(POD)活性,催化H2O2产生羟基自由基(·OH),并且可以通过近红外(NIR)光照射进一步增强。此外,制备的ETN呈蜂窝状结构,可作为一种纳米海绵促进血液凝固。这些特性使ETN成为一种多功能材料,促进感染伤口的愈合。相关研究成果以"An Erythrocyte-Templated Iron Single-Atom Nanozyme for Wound Healing"为题在线发表于《Advanced Science》杂志。
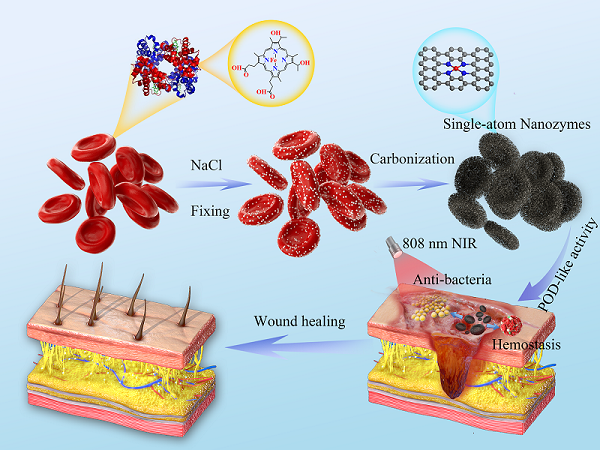
图1. 以红细胞为模板制备的单原子纳米酶促进感染伤口愈合
中国科学院生物物理研究所高利增研究员和北京交通大学张金华教授为论文通讯作者,中国科学院生物物理研究所博士研究生王晓楠、暨南大学与北京交通大学联合培养博士生刘婷为本文共同第一作者,中国科学院生物物理研究所范克龙研究员为该研究给予了指导和帮助。该研究得到国家重点研发计划、国家自然科学基金等项目的资助。
文章链接:https://doi.org/10.1002/advs.202307844
发布时间:2023年12月12日(供稿:高利增研究组)
 附件下载:
附件下载: